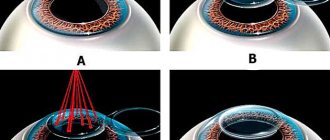
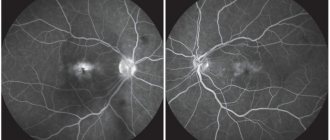
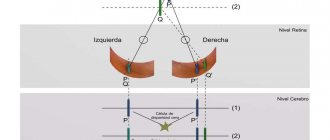
Метод оптической когерентной томографии (ОКТ) позволяет прижизненно визуализировать структуры глаза в поперечном срезе. Разрешение этой методики очень высокое, поэтому ее сравнивают по информативности с морфологическим исследованием (при помощи микроскопа). В основе ОКТ лежит принцип низкокогерентной интерферометрии.
Оптическая когерентная томография показывает величину и глубину проникновения светового сигнала, который отражается от тканей организма, отличающихся по оптическим свойствам. Осевое разрешение ОКТ составляет около 10 мкм, что является лучшим из всех существующих методик исследования биологических структур. При оптической когерентной томографии определяется эхо-задержку световой волны, отраженной от тканей. При этом производится измерение глубины и интенсивности сигнала. Во время фокусировки на тканях световой луч рассеивается и частично отражается от микроструктур исследуемых тканей на разных уровнях.
Этот механизм напоминает принцип, используемый при ультразвуковом А-сканировании, во время которого измеряют время прохождения акустической волны от источника до тканей и в обратном направлении к воспринимающему устройству. При оптической когерентной томографии используется не звуковая волна, а пучок когерентного света в инфракрасном диапазоне (820 нм).
Схема используемого в офтальмологической практике аппарата для ОКТ выглядит следующим образом. Источник пучка света представлен суперлюминесцентным диодом, длина когерентности в котором составляет 5-20 мкм. Интерферомер Майкельсона находится в аппаратной части прибора, конфокальный микроскоп (щелевая лампа или фундус-камера) находятся в объектном плече, а блок временной модуляции – в опорном плече. При помощи видеокамеры траектория сканирования и общая картина выводятся на монитор. Для обработки полученных значений используется компьютер, который представляет данные в виде графических файлов. Томограммы изначально выглядят как черно-белые логрифимические шкалы. Чтобы проще было воспринимать полученные картины, их преобразуют в псевдоцветные, в которых используется черный цвет для оптической прозрачности и красный/белый цвет для участков с высокой степенью светоотражения.
Область применения
Современная оптическая когерентная томография является бесконтактной и неинвазивной методикой, которую в офтальмологической практике используют с целью изучения морфологических структур переднего и заднего отрезка глаза у живых пациентов. Эта методика позволяет не только выявить, но и количественно оценить, а также записать показатели сетчатки, зрительного нерва. При этом измеряется толщина и определяется прозрачность роговицы, исследуется структура радужки. ОКТ можно повторить много раз, а результаты сохраняются в памяти компьютера, что удобно для оценки течения патологического процесса.
Показания
Оптическая когерентная томография проводится для того, чтобы получить информацию обо всех структурах глаза, как нормальных, так и патологических.
При помощи ОКТ можно диагностировать многие офтальмологические заболевания:
- глаукома
- иридоцилиарная дистрофия
- изменения после рефракционных операций
- разрывы и предразрывы макулы
- тракционный витреоретинальный синдром
- отек и дистрофия макулы
- пигментный ретинит
В каких случаях показана процедура
КТ сетчатки глаза проводится при подозрениях или в случае наличия таких болезнях, как:
- дистрофия сетчатки;
- макулодистрофия;
- глаукома;
- пигментный ретинит;
- заболевания зрительного нерва, роговицы;
- макулярные отёки;
- тромбоз;
- сахарный диабет;
- опухоль;
- разрыв аневризмы.
При жалобах на снижение зрения и боли в глазах рекомендуется провести пациенту ОКТ глаз
Кроме того, пациентам проводится такое исследование при разрывах, отслоении сетчатки, до или после хирургического вмешательства и в случае помутнения роговицы неясного происхождения.
Процедура также выполняется, если пациент жалуется на определённые симптомы. Это может быть появление мушек перед глазами, болевые ощущения в органе, снижение остроты зрения или резкое его пропадание.
Методика и последующий уход
Технические аспекты ОКТ включают следующие этапы. Сначала проводят ввод данных пациента и начинают обследование. При этом пациента просят зафиксировать взор на мерцающем объекте (в линзе фундус-камеры). Далее камеру постепенно приближают к глазу, пока изображение сетчатки на мониторе ни станет четким. Врач фиксирует камеру на этом расстоянии при помощи специальной кнопки и дополнительно регулирует резкость изображения. При низкой остроте зрения (когда пациент не может увидеть мерцающий объект) нужно использовать внешнюю подсветку, при этом пациент должен смотреть прямо перед собой. Обычно расстояние от глаза до линзы камеры составляет 9 мм. ОКТ проводят путем сканирования, процесс этот контролируют при помощи панели управления, которая состоит из шести групп кнопок и манипуляторов с разной функцией.
После сканирования выполняют выравнивание изображений и очищение их от шумов. По полученным данным проводят измерение тканей и анализ оптической плотности. Количественные измерения можно сравнивать с нормальными показателями, которые были сохранены в памяти компьютера.
Как нужно подготовиться пациенту
Специальной подготовки к компьютерной томографии глаз проводить не требуется. Однако в целях получения более качественного изображения врачи рекомендуют выполнить расширение зрачка. Для этого в глаза пациенту закапывают специальный медикамент.
После диагностики с контрастом может появиться покраснение и зуд в глазах
В некоторых случаях требуется проведение МСКТ орбиты глаза с контрастом. Для данной процедуры используют йодосодержащее вещество. Перед таким исследованием пациенту нельзя есть в течение четырёх часов. При наличии аллергии (даже на что-либо) следует обязательно об этом сообщить врачу, поскольку иногда выполнение процедуры с контрастом вызывает негативную реакцию в виде покраснений и зуда.
Интерпретация
Постановка диагноза всегда основывается на экспертном анализе сканограмм, полученных при ОКТ. При этом врач обращает внимание на морфологические показатели тканей (взаимоотношение слоев и отделов, изменение внешнего контура, взаимоотношение с соседними тканевыми структурами), изменение светоотражающей способности (снижение или повышение прозрачности, присутствие патологических включений). При количественном анализе данных можно увидеть изменение толщины слоя клеток (истончение, утолщение), объема изучаемой структуры, а также получить карту поверхности.
ОКТ при глаукоме
Первым признаком патологического действия повышенного внутриглазного давления (ВГД) при глаукоме является измерение диска зрительного нерва, которое может быть диагностировано с помощью указанной методики.
На данный момент оптическая когерентная томография является «золотым стандартом» в диагностике глаукомы, т.к. позволяет с намного большей точностью установить диагноз, чем при использовании тонометрии, тонографии, определении полей зрения и т.д.
Другие структуры глаза и заболевания, при которых применяется исследование:
Томография роговицы
При ОКТ роговицы важно правильно расположить все структурные отклонения, а также рассчитать их показатели. Это поможет выбрать оптимальную тактику лечения или оценить его эффективность. В некоторых ситуациях только при помощи оптической когерентной томографии можно рассчитать толщину роговицы. При этом очень важно, что методика является бесконтактной и не оказывает влияния на поврежденный роговичный слой.
Томография радужки
При этом врач может рассмотреть передний прозрачный слой, пигментный эпителий и собственно стромальное вещества. Все эти слои имеет разную отражающую способность, что связано с разной концентрацией пигмента в их клетках. Если радужка светлая, то в наибольшей степени отражение происходит от заднего слоя пигментного эпителия (при этом два передних слоя визуализируются недостаточно). При ранних патологических процессах в радужке, которые можно выявить при ОКТ, диагностируют ряд заболеваний глаз (синдром пигментной дисперсии, эссенциальная мезодермальная дистрофия, псевдоэксфолиативный синдром, синдром Франк-Каменецкого.
Томография сетчатки
При оптической когерентной томографии здорового глаза можно выявить правильный профиль макулы, в центре которой имеется углубление. Слои сетчатки различаются в зависимости от их способности отражать световые лучи, они не имеют очаговых изменений и равномерные по величине. Слой нервных волокон, пигментный эпителий относятся к слоям с высокой светоотражающей способностью, плексиформный и ядерный слои – со средней, фоторецепторный слой практически прозрачный. Вдоль наружного края сетчатки располагается ярко-красный высокофоторефлектирующий слой, толщиа которого составляет 70 мкм. Он состоит из хориокапилляров и пигментного эпителия сетчатки. Темная полоса, расположенная рядом с красной, является фоторецепторным слоем.
На внутренней поверхности также имеется ярко-красная линия, соответствующая нервным волокнам. За счет наличия такого резкого окрашивания слоев сетчатки, врач легко может измерить их толщину. В зоне центральной фовеальной ямки толщина сетчатки составляет около 162 мкм, а у края фовеа – 235 мкм.
Идиопатические разрывы макулы
При идиопатических дефектах сетчатки в районе желтого пятна, которые возникают без видимых причин в пожилом возрасте, при ОКТ можно выявить признаки заболевания на всех этапах клинического течения, а также определиться с тактикой лечения и осуществлять контроль за ним. При начальных проявлениях (предразрыв) на томограммах видна фовеальная отслойка в зоне нейроэпителия, что связано с витреофовеолярной тракцией. Если имеется ламеллярный разрыв, то на томограмме виден дефект внутренней поверхности сетчатки, а фоторецепторный слой сохранен. При сквозном разрыве дефект распространяется на всю толщу сетчатки.
Дегенеративные изменения
При оптической когерентной томографии вокруг зоны разрыва можно выявить дегенеративные трансформации сетчатки. Формирование витреомакулярных тракций также является важным прогностическим симптомом. Анализируя томограмму, нужно измерить толщину сетчатки в зоне макулы, диаметры разрыва (минимальный и максимальный), размер интраретинальных кист, толщину отечной ткани по краю разрыва. Также важно обращать внимание на степень дегенерации тканей около разрыва, которые проявляются уплотнением и красным их окрашиванием на изображении.
Возрастная макулодистрофия
Эта группа хронических заболеваний с неизвестной этиологией проявляется дегенеративными нарушениями в сетчатки у пожилых пациентов. При ОКТ можно обследовать изменения структур в заднем полюсе глаза. Доктор измеряет толщину сетчатки, чтобы оценить эффективность лечения.
Диабетический отек макулы
Заболевания развивается на фоне сахарного диабета и протекает довольно тяжело. На томограммах измеряют толщину сетчатки, оценивают степень дегенерации тканей, интраретинальные включения и состояние витреомакулярного пространства.
Зрительный нерв
Оптическая когерентная томография с высокой точностью позволяет визуализировать нервные волокна и измерить толщину зрительного нерва. Этот показатель коррелирует с его функцией, в том числе с сохранностью поля зрения. Нервные волокна обладают высокой степенью обратного рассеивания, поэтому хорошо контрастируются с промежуточными слоями сетчатки. Аксоны традиционно ориентированы перпендикулярно пучку света от томографа.
Для исследования диска зрительного нерва используют радиальные или кольцевые сканы. В первом случае изображение диска представлено в поперечном сечении, это дает возможность оценить экскавацию, толщину нервных волокон в околососочковой области угол наклона волокон по отношению к сетчатке и поверхности диска.
Для получения трехмерных изображений диска зрительного нерва, нужно провести серию съемок в различных меридианах. При этом можно оценить структуру волокон на разных участках диска. Такая томограмма выглядит как плоский линейный снимок. Обычно толщина сетчатки и волокон рассчитывается компьютером и представляется на экране в виде усредненной величины для всей области изучения, только квадранта, часа или же для каждого скана в отдельности. Все эти количественные показатели сравниваются с нормальными значениями, а также с величинами, полученными в ходе предыдущих исследований. При этом можно выявить диффузную атрофию, локальные дефекты, что применяется для диагностики нейродегенеративных заболеваний.
Застойный диск
Застойный диск свидетельствует о повышении внутричерепного давления. При ОКТ довольно просто выявить признаки застойного диска, измерить его параметры и оценить изменения в динамике. Для этого исследуют уровень светоотражения тканей, так как оно изменяется в зависимости от их гидратации и дегенерации.
Ямка зрительного нерва
Эта врожденная аномалия развития чаще всего приводит к расслоению сетчатки в макулярной зоне (шизис). При ОКТ четко определяются дефекты диска зрительного нерва, расслоение вещества сетчатки и другие изменения, происходящие в зоне желтого пятна.
Пигментный ретинит
Тапеторетинальная абиотрофия относится к наследственным заболеваниям с прогрессирующим течением. При этом происходит поражение фоторецепторного слоя. ОКТ используют для оценки хориоретинального комплекса и определения тяжести заболевания. На томограммах измеряют толщину фоторецепторного, нейроглиального слоев и диаметр нервных волокон, оценивают прозрачность тканей сетчатки. Даже при латентном течении пигментного ретинита, когда отсутствуют клинические симптомы заболевания, при ОКТ можно выявить характерные изменения, представленные уменьшением толщины фоторецепторного слоя, снижением прозрачности этого слоя, а также появлением признаков повышенного метаболизма пигментного эпителия. При сравнении томограмм можно осуществлять мониторинг за патологчисекими изменениями. Также при ОКТ диагностируют беспигментную форму пигментного ретинита у детей, когда провести функциональные методы обследования не представляется возможным.
Спектральная оптическая когерентная томография: принципы и возможности метода
and possibilities (Literary review) A.V. Svirin, Yu.I. Kiiko*, B.V. Obruch, A.V. Bogomolov Russian State Medical University of Roszdrav, *FGU VCGPH of Roszdrav, Moscow
Authors discuss principles, diagnostic possibilities and types of new examination method – spectral optic coherent tomography which information value exceeds the OCT’s.
Оптическая когерентная томография (ОКТ) широко используется в современной медицине. Это неинвазивный и высокоточный метод исследования, с помощью которого стало возможным получать изображение поперечного среза исследуемых тканей in vivo. ОКТ была разработана в Массачусетском технологическом университете в конце 80–х годов ХХ века. ОКТ нашла применение во многих отраслях медицины – в гастроэнтерологии, кардиологии, урологии, дерматологии, стоматологии. Однако наибольшую популярность новая методика завоевала в диагностике заболеваний глаза. Самый известный прибор, реализующий технологию ОКТ в офтальмологии – Stratus OCT (Carl Zeiss Meditec) на данный момент был продан в количестве, превышающем 6 тыс. экземпляров. В мире насчитывается более тысячи статей и научных трудов, посвященных применению ОКТ в диагностике заболеваний глаза. Принципы метода Суть ОКТ заключается в измерении времени задержки светового луча, отраженного от исследуемой ткани. Поскольку современное оборудование не позволяет непосредственно измерять этот параметр на столь малых пространственных отрезках, работа ОКТ построена на принципах световой интерферометрии. До недавнего времени основой всех когерентных томографов был интерферометр Михельсона (time–domain OCT). Источником света в нем является суперлюминесцентный диод, позволяющий получать луч низкой когерентности. С помощью делителя световой пучок расщепляется на две равные части, одна из которых направляется на исследуемую структуру, вторая – на подвижное зеркало (опорное плечо). Исследователь путем смещения рабочей части прибора добивается того, чтобы расстояние до обоих объектов было одинаковым. После этого отраженные лучи суммируются, что вызывает эффект интерференции, регистрируемый фотодетектором. Полученная амплитуда интерферировавшей световой волны характеризует отражающую способность конкретной точки исследуемого объекта. Затем опорное плечо смещается и выполняется исследование следующей точки. В итоге формируется одномерный А–скан (axial scan). Получаемое путем суммирования нескольких А–сканов двухмерное изображение, по аналогии с ультразвуковым исследованием, называется В–сканом. Расстояние между точками А–скана определяет продольное (аксиальное) разрешение, между соседними А–сканами – поперечное. Основным фактором, ограничивающим возможности Time–domain OCT, является наличие механического элемента системы – подвижного зеркала опорного плеча. От точности и скорости его смещения напрямую зависят аксиальное разрешение и время сканирования. Максимальная продольная разрешающая способность ОКТ, полученная в лабораторных условиях, составляет 2–3 мкм. Этот результат достигнут на неподвижных объектах с использованием в качестве источника света фемтосекундного лазера. Однако коммерческий вариант данной системы не был реализован ввиду ее высокой стоимости. Максимальная разрешающая способность Time–domain ОКТ в клинике представлена в последней модификации Stratus OCT и составляет 8–10 мкм при скорости сканирования 400 А–сканов в секунду. Стандартное исследование, состоящее из 512 А–сканов, занимает, таким образом, более 1 секунды. Спектральная ОКТ Коренной перелом в технологии оптической когерентной томографии произошел с внедрением в практику спектральных интерферометров, использующих преобразование Фурье (spectral/Fourier domain). Их отличием от интерферометра Михельсона является наличие спектрометра и высокоскоростной CCD – камеры (CCD – charge–coupled device, русскоязычный аналог термина – ПЗС (прибор зарядовой связи). Источником света является широкополосный суперлюминесцентный диод, позволяющий получить низкокогерентный луч, содержащий несколько длин волн. Как и в time–domain OCT, световой импульс делится на две равные части, одна из которых отражается от фиксированного опорного плеча (зеркала), вторая – от исследуемого объекта. Затем сигналы суммируются, а проинтерферировавший луч света раскладывается на составные части спектра, которые одномоментно фиксируются CCD–камерой. Полученный спектр интерференции состоит из совокупности световых волн, отраженных от различных по глубине участков исследуемого объекта. Затем из полученного массива данных путем математического преобразования Фурье выделяются частотные составляющие, из которых формируется А–скан. Таким образом, получение линейного скана происходит не путем последовательного измерения отражающих свойств каждой отдельной точки пространства, а одномоментно. Глубина сканирования при этом равна зоне когерентности. Подобный принцип исследования позволяет преодолеть ограничивающие факторы, связанные со скоростью и точностью движения механических частей интерферометра, поскольку опорное плечо остается во время исследования неподвижным. Скорость сканирования спектральных ОКТ зависит от быстроты работы CCD–камеры и математического преобразователя, а аксиальная разрешающая способность – от чувствительности спектрометра. Поперечное разрешение всех типов ОКТ ограничивается аберрациями оптической системы глаза. Благодаря принципу своей работы, спектральные ОКТ позволяют выполнять более 25 тыс. линейных сканов в секунду, превосходя по этому параметру оптические томографы предыдущего поколения более чем в 60 раз (некоторые модели – в 120 раз). Аксиальная разрешающая способность находится в пределах 3–8 мкм, поперечная – 10–15 мкм. К моменту написания статьи на мировом рынке было представлено 5 моделей спектральных оптических когерентных томографов c возможностью исследования заднего отрезка глаза: 1) RTVue–100 фирмы Optovue (США) – позволил совместить в одном приборе возможности исследования как переднего, так и заднего отрезка глазного яблока; 2) 3D OCT–1000 (Topcon) – обладает функциями фундус–камеры и сопоставления фотоснимка глазного дна с ОКТ изображением; 3) CIRRUS HD OCT (Carl Zeiss); 4) Soct Copernicus и Soct Copernicus HR совместного производства Reichert (США) – Optopol (Польша). Soct Copernicus HR обладает на сегодняшний день максимальной заявленной скоростью сканирования (55000 А–сканов в секунду) и аксиальным разрешением (3 мкм). Также под маркой Soct разработан спектральный ОКТ для исследования переднего отрезка глаза; 5) Spectralis HRA+OCT (Heidelberg Engineering) – ОКТ–приставка к лазерному сканирующему ангиографу HRA. Первым коммерческим прибором, в котором были реализованы возможности спектральной ОКТ глаза, стал RTVu–100 фирмы Optovue (США). Компания объявила о начале его производства в конце 2006 г. Именно этот прибор мы используем в работе нашей клиники, поэтому в дальнейшем основные технические характеристики и протоколы обследования приводятся исходя из возможностей RTVu–100. Улучшенные диагностические возможности Значительный прирост скорости и точности метода качественно изменил роль оптической когерентной томографии в диагностике заболеваний глаза. Чтобы понять всю значимость этих изменений, рассмотрим спектральную ОКТ с точки зрения ее клинического применения. Одной из самых главных проблем, возникающих при использовании томографов предыдущего поколения, является чувствительность метода к микродвижениям глазного яблока. Наибольшие погрешности вызывают так называемые микросаккады – непроизвольные быстрые движения с амплитудой 2–10 угловых мин и интервалом от 100 мс. Одно стандартное исследование на Stratus OCT (512 А–сканов) длится 1,28 сек. – за это время глазное яблоко 10–14 раз меняет свое положение. Подобный эффект негативно сказывается на конечной томограмме. Для нейтрализации появляющихся артефактов применяются методы графического сглаживания. Они эффективно выравнивают изображение, но могут скрывать локальные изменения, что вносит дополнительные затруднения в интерпретацию результатов. Спектральные когерентные томографы в отличие от time–domain OCT позволяют получить стандартный линейный профиль (1024 А–сканов) в среднем за 0,04 сек. За этот промежуток времени глазное яблоко не успевает совершить значимых движений, а значит, конечный В–скан максимально соответствует истинной структуре изучаемого объекта. Высокое разрешение позволяет четко идентифицировать все слои сетчатки и внутренние слои сосудистой оболочки. Диагностический поиск производится на уровне отдельных структур и групп клеток (рис. 1). Четкая визуализация комплекса «пигментный эпителий – слой фоторецепторов – наружная пограничная мембрана» способствует раннему выявлению ретино–хориоидальной патологии. В качестве примера на рисунке 2 представлена ОКТ периферической зоны сетчатки пациента, страдающего дистрофией Штаргардта. Высокая разрешающая способность метода позволяет выявить патологические изменения в слое наружных сегментов фоторецепторов. Трехмерная визуализация Однако главным отличием спектральных ОКТ стала возможность трехмерной визуализации объекта (участок сетчатки, головка зрительного нерва, роговица и проч.). Высокая скорость сканирования позволяет выполнить большое количество А–сканов (более 50 000) участка ткани фиксированной площади за 1–2 с. На основе этих данных программное обеспечение восстанавливает трехмерную структуру объекта. Полученное 3D–изображение позволяет оценить профиль поверхности изучаемой структуры, ее внутреннюю топографию. Возможна четкая визуализация границ патологических образований, наблюдение за их динамикой. Также эта функция незаменима в поиске небольших по размерам изменений, вероятность попадания которых в одиночный линейный скан мала. На рисунке 3 продемонстрирована трехмерная структура центральной зоны сетчатки пациентки с хориоидальной неоваскуляризацией. 3D–томограмма позволяет оценить вовлеченность фовеолы в патологический процесс и проследить динамику изменений. Трехмерная модель головки зрительного нерва (ГЗН) открывает новые возможности в оценке профиля экскавации при глаукоме (рис. 4). RTVu–100 позволяет выполнять морфометрию ГЗН, сходную по структуре получаемых данных с HRT. При этом определение границ диска зрительного нерва производится на основе 3D–изображения, что позволяет наносить его контур, основываясь на структурных особенностях ГЗН. Функции картирования Возможность исследования толщины сетчатки и ее слоев на определенном участке впервые была реализована в Stratus OCT. Итогом выполнения стандартного протокола является карта, представляющая полученные результаты графически и в абсолютных значениях. Методы картирования нашли широкое применение как в практической, так и в научно–исследовательской работе. Спектральная оптическая томография предоставляет новые возможности построения карт глазных структур. Прежде всего высокая скорость сканирования повышает их точность, поскольку на единицу площади приходится большее количество А–сканов. Кроме того, выполнение стандартного протокола исследования занимает не более 1 с, следовательно, движения глазного яблока оказывают минимальное воздействие на конечный результат. Высокая разрешающая способность позволяет четко идентифицировать границы между слоями сетчатки в автоматическом режиме. В результате становится возможным получать не только карту толщины сетчатки, но и ее отдельных слоев (слой ганглиозных клеток и нервных волокон, фоторецепторных клеток, пигментного эпителия). На рисунке 5–1 представлена карта элевации пигментного эпителия сетчатки пациентки с впервые диагностированной ВМД. Линейные сканы центральной зоны сетчатки не выявили патологических изменений. Однако методом картирования парацентрально были обнаружены участки локальной элевации пигментнго эпителия. Линейный скан, выполненный прицельно, позволил выявить расположенные на периферии друзы (рис. 5–2). Карта толщины слоя нервных волокон и ганглиозных клеток сетчатки расширяет возможности прибора в диагностике атрофий зрительного нерва, в том числе глаукомного генеза. Можно провести параллель в структуре получаемых результатов с поляриметрическими методами (хотя в последних определяется только толщина слоя нервных волокон без учета слоя ганглиозных клеток). Заключение К сожалению, в рамках одной статьи невозможно описать все новые возможности, которые предоставляет исследователю спектральная оптическая когерентная томография. Еще предстоит выработать комплекс диагностических критериев для основных групп заболеваний заднего отрезка глаза, оценить точность получаемых результатов относительно приборов, использующих другие физические принципы (сканирующие лазерные офтальмоскопы, лазерные поляриметры и т.п.). Однако уже сейчас можно утверждать, что спектральная оптическая когерентная томография является качественно новым методом диагностики заболеваний глаз. Ее информативность значительно превосходит ОКТ предыдущего поколения за счет возросшей разрешающей способности и высокой скорости исследования. Метод позволяет получить исчерпывающее представление об ультраструктуре произвольного участка сетчатки и головки зрительного нерва. Разнонаправленность получаемых результатов, широкие возможности диагностики и динамического наблюдения различных глазных заболеваний делают спектральную оптическую когерентную томографию одним из наиболее точных и универсальных методов морфологического исследования в офтальмологии.
Операционные характеристики
Источником светового сигнала в оптическом когерентном томографе является суперлюминесцентный диод (длина волны 820 нм используется для изучения сетчатки, 1310 нм – для переднего отрезка глаза). Тип сигнала при ОКТ представляет собой оптическое рассеивание от ткани. Размер поля изображения зависит от области изучения: для заднего отрезка он составляет 30 на 22 мм, для переднего – 10 на 16 мкм. Разрешение метода для продольных структур достигает 10 мкм, а для поперечных – 20 мкм. Скорость сканирования при ОКТ достигает 500 срезов в секунду.