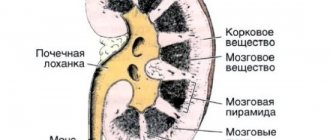
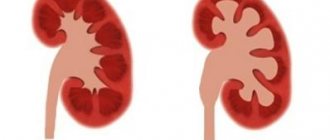
Пороки развития половых органов
Диагностика простых вариантов порока не представляет сложностей. Стандартное обследование при подозрении на непроходимость влагалища и шейки матки, помимо общеклинических и лабораторных исследований, включает сбор анамнеза, оценку физического и полового развития, осмотр наружных половых органов, бактериологическое и бактериоскопическое исследование выделений из половых путей, ректально-абдоминальное исследование, зондирование влагалища, УЗИ половой и мочевой систем. Как правило, этих исследований достаточно для точного определения варианта порока и выбора метода оперативного вмешательства.
При объективном обследовании преддверие влагалища и девственная плева выглядят обычно. Даже при тотальной аплазии влагалища его преддверие сохранено. Только при атрезии девственной плевы ее вид отличается от обычного. При надавливании на переднюю брюшную стенку над лоном девственная плева выбухает в виде цианотичного купола.
Бактериологическое и бактериоскопическое исследование выделений из половых путей дают существенную информацию в основном при свищевой атрезии влагалища, когда гнойные выделения служат косвенным диагностическим признаком, а результаты анализов необходимы для проведения рациональной антибактериальной терапии.
Пальпируемое при ректально-абдоминальном исследовании округлое эластичное малоболезненное и малоподвижное образование, оттесняющее матку кверху, обычно является гематокольпосом. Давление на гематокольпос через прямую кишку передается на матку и ощущается при пальпации над лоном. Смещаемость гематокольпоса ограничена, чем он отличается, например, от кисты яичника, похожей локализации, консистенции и формы.
Зондирование влагалища имеет целью определение глубины нижнего отдела влагалища и проводится одновременно с ректально-абдоминальным исследованием. Расстояние от верхушки купола влагалища до дна гематокольпоса позволяет точно определить диастаз между отделами влагалища, оценить запасы пластического материала и наметить план операции. Дистальная часть влагалища часто представлена одним преддверием и имеет глубину около 1-2 см. Реже углубление за девственной плевой бывает менее 1 см.
Ультразвуковое исследование (УЗИ) внутренних гениталий документально подтверждает правильность трактовки клинических данных. Исследование проводят при наполненном мочевом пузыре с расположением датчика над лоном и в области промежности. Попутно осматривают органы брюшной полости и забрюшинного пространства. УЗИ позволяет достоверно определить размеры матки и ее полости, толщину эндометрия, размеры и толщину стенок гематокольпоса, расстояние от его дна до кожи промежности. Вместе с тем достоверность УЗИ достаточно высокая лишь в диагностике наиболее простых форм порока — низких атрезии влагалища без удвоения органов. Во всех сомнительных случаях — при несовпадении данных анамнеза, клинической картины и результатов обследования данные УЗИ следует проверять другими методами — эндоскопией, магнитно-резонансной томографией (МРТ). В некоторых наблюдениях наиболее информативны лапароскопия и вагинография.
В диагностике сложных или нетипичных пороков развития влагалища следует отдавать предпочтение магнитно-резонансной томографии. Специальной подготовки к МРТ не требуется. Исследование проводят в положении пациентки на спине во фронтальной, сагиттальной и аксиальной проекциях. При атрезиях и аплазиях влагалища наиболее информативна для уточнения анатомического строения сагиттальная проекция, позволяющая точно определить величину диастаза между отделами влагалища, размеры гематометры и гематокольпоса, оценить состояние шейки матки. Однако при удвоении влагалища и матки сагиттальные срезы не позволяют достаточно легко реконструировать анатомические взаимоотношения органов. В случае удвоения половых путей более информативно исследование во фронтальной проекции. В распознавании многих сложных аномалий внутренних половых органов МРТ представляет наиболее ценную информацию, предопределяющую выбор оперативного вмешательства.
Данные УЗИ и МРТ при свищевой форме непроходимости влагалища могут различаться в зависимости от времени проведения исследования и степени заполнения влагалища содержимым. Опорожнение обычно происходит во время ректально-абдоминального исследования. Пиокольпос может опорожняться спонтанно на фоне противовоспалительной терапии. Ошибочная трактовка данных МРТ возможна при «пустом» влагалище.
В диагностике «пустого» влагалища при свищевых формах ат-резии вагинография более информативна, чем УЗИ и МРТ. До появления УЗИ и МРТ вагинография была единственным исследованием полости влагалища выше уровня обструкции. Однако вагинография связана с высоким риском инфицирования проксимального отдела влагалища при замкнутом гематокольпосе. В настоящее время вагинографию целесообразно использовать лишь при свищевой форме атрезии влагалища в качестве документирующего исследования.
Эндоскопические исследования нижних мочевых путей (синусо-уретроцистоскопия), как и уродинам и ческие исследования, показаны детям с сочетанной мочеполовой патологией (ятрогенные повреждения уретры, персистирующий урогенитальный синус, клоакальные аномалии).
Таким образом, уточнение анатомии порока развития, необходимое для выбора хирургической тактики, возможно лишь при комплексном обследовании, включающем рентгенологические и эндоскопические методы. МРТ остается наиболее информативным клиническим методом исследования органов малого таза.
Диагностические трудности при непроходимости влагалища и шейки матки подтверждаются высокой частотой и разнообразием диагностических ошибок, совершаемых как гинекологами, так и врачами других специальностей.
Первичный этап диагностики при врожденной непроходимости влагалища и шейки матки практически всегда вызывает затруднение и редко завершается установлением правильного диагноза. Заболевание часто проявляет себя весьма неожиданно, начинается с острых болей в животе, задержки мочи или появления опухолевидного образования в брюшной полости, которые нередко становятся причиной срочной лапаротомии.
Многим девочкам-подросткам с врожденной непроходимостью влагалища сначала выполняют аппендэктомию по поводу подозрения на острый аппендицит и лишь затем им устанавливают правильный диагноз. Это обусловлено резкими болями в животе, часто не оставляющими у хирурга сомнений в необходимости экстренной операции. Избежать неоправданных аппендэктомий позволяет УЗИ.
К тяжелым последствиям может привести неверная диагностика мукокольпоса у грудных детей. Подозрение на опухоль или кисту брюшной полости провоцирует хирурга на выполнение широкой лапаротомии с удалением верхнего отдела влагалища.
Острая задержка мочи или примесь гноя в моче (пиурия), встречающаяся при свищевом пиокольпосе, требует урологического обследования. Ребенок может надолго стать «путешественником» по урологическим стационарам.
Часто встречаются ошибки при полном удвоении матки и аплазии или атрезии одной половины удвоенного влагалища. Наиболее сложно определить второе замкнутое влагалище, когда имеются две почки, так как полное удвоение матки и добавочное замкнутое рудиментарное влагалище сопровождаются агенезией одной почки.
В связи с острыми болями внизу живота при непроходимости влагалища нередко вскрывают гематокольпос и эвакуируют его содержимое. Подобное вмешательство, особенно при высоком гематокольпосе, связано со значительным риском повреждения уретры, мочевого пузыря и прямой кишки и может привести к развитию пиокольпоса, пиометры и перитониту. Экстренных показаний для опорожнения гематокольпоса не существует. Женские половые пути имеют большие адаптационные возможности, и обезболивающей терапии (баралгин, максиган) бывает достаточно для ослабления или купирования болевого синдрома. Оперативные вмешательства могут выполнять только специалисты, желательно у пациенток в межменструальном периоде.
Факторы риска развития врожденных аномалий органов мочевой системы
Введение. Врожденные пороки развития (ВПР) органов мочевой системы (ОМС) составляют более 50% всех аномалий развития брюшной полости у новорожденных и возникают примерно в 0,5% всех беременностей [1,2]. Несмотря на развитие пренатальной диагностики и возможности раннего хирургического вмешательства, аномалии развития ОМС по прежнему являются главной причиной развития почечной недостаточности у новорожденных [3,4]. Развитие профилактической и превентивной нефрологии является приоритетным направлением в педиатрии и основано на распознавании факторов риска (ФР) заболеваний ОМС, оценке риска инвалидизации и проведении комплекса мероприятий по профилактике заболеваний почек, ранней диагностике врожденной патологии ОМС и реабилитации больных [5-8]. Накопление данных об отдельных ФР, способствующих развитию патологии почек, дает возможность противостоять этой патологии путем контролирования ФР у детей на стадии пограничных состояний [9]. Для этого необходимо знать частоту патологии почек, региональные особенности ФР у детей с учетом возраста, пола, наследственных факторов, экзогенных воздействий [10,11]. Отсутствие однозначной оценки этиологического и патогенетического значения факторов, влияющих на формирование врожденных пороков развития почек (ВПРП) и эффективности клинико-прогностических критериев возникновения ВПРП определило цель и задачи настоящей работы.
Цель исследования: повышение эффективности ранней диагностики и прогнозирования ВПРП на основании оценки значимости факторов риска.
Задачи исследования:
1. Оценить роль социально-бытовых факторов в формировании ВПР ОМС.
2. Изучить роль наследственных факторов в формировании ВПР ОМС.
3. Определить роль акушерско-гинекологического анамнеза в формировании ВПР ОМС.
Материалы и методы. Обследовано 130 детей, которые были разделены на 3 группы: в 1-ю группу вошли 50 детей с пузырно-мочеточниковым рефлюксом (ПМР), 2-ю группу составили 40 детей с гидронефрозом, тогда как в 3 группу вошли 40 здоровых детей. На первом этапе обследования детей использован метод анкетирования родителей по специально разработанной анкете для выявления социальных и медико-биологических факторов риска, в том числе управляемых, малоуправляемых и неуправляемых, а также социально-гигиенических факторов условий и образа жизни семьи; проведены анализ генеалогического, медико-биологического анамнеза, оценка физического и полового развития. Сбор информации о каждом ребёнке дополнялся данными из учётной медицинской документации, а также данными из архива родильного дома. В анкету входили вопросы, касающиеся порядкового номера беременности, возраста родителей, профессиональные вредности до рождения ребенка у родителей, заболевания матери во время беременности, осложнения во время беременности, прием лекарственных препаратов во время беременности, срок родоразрешения и наследственной отягощенности.
Результаты исследования. Некоторые нозологические формы ВПР ОМС связаны с дополнительными социально-бытовыми факторами, которые реализуются, как через женщин, путем прямого влияния на плод во время беременности, так и через мужчин, оказывая мутагенное влияние на сперматогенез. Зависимость состояния ребенка от возраста родителей, в котором произошло его зачатие, хорошо известна. В нашем исследовании во всех 3-х группах преобладал возраст родителей от 18 до 40 лет, и составил в группе с ПМР 70,0% у матерей и 86,0% у отцов, в группе с гидронефрозом 67,5% и 87,5% у матери и отца соответственно и в контрольной группе 72,5% и 77,5% соответственно. Было выявлено, что у детей с гидронефрозом статистически значимо чаще возраст матерей был старше 40 лет (p<0,05), что подчеркивает необходимость тщательного наблюдения за детьми, рожденными от матерей в данной группе риска (табл. 1). В формировании ВПР определенную роль играют профессиональные вредности родителей. При анализе производственных вредностей были получены следующие результаты: у детей I и II групп матери статистически значимо чаще работали на производстве, связанном с воздействием солей тяжелых металлов, а также химических факторов, тогда как в контрольной группе не было выявлено подобной тенденции (p<0,05) (табл. 1). При этом работа, связанная с воздействием высоких температур, производственной пыли, вибрации, а также связанная с тяжелым физическим трудом не оказывает статистически значимого воздействия на формирование ВПР ОМС.
Таблица 1. Дородовые факторы риска развития пороков органов мочевой системы.
Примечание: здесь и далее * — p<0,05 – статистически значимые различия между 1-й, 2-й и контрольной группами.
Также нами был проанализирован семейный анамнез. Было выявлено, что ведущими ФР формирования заболеваний ОМС у детей являются наличие заболеваний почек в семье, особенно у матери. Так, у родственников детей с ПМР поликистоз встречался чаще, чем другие пороки почек, также часто встречался гидронефроз, тогда как такие пороки почек как единственная почка, удвоение почки, гипоплазия, дистопия и ротация, сращенная почка и солитарная киста практически не встречались. У детей с ПМР статистически значимо чаще встречались пороки почек у матерей (32%), чем бабушек и дедушек (p<0,05). У детей с гидронефрозом родственники статистически значимо чаще болели гидронефрозом (p<0,05), тогда как другие пороки развития практически не встречались. При этом гидронефрозом чаще болели женщины (мамы, бабушки, сестры). У детей 3 группы не было выявлено статистически значимых различий при анализе наличия пороков ОМС в анамнезе. Особенности акушерско-гинекологического анамнеза, течения беременности определяют характер внутриутробного развития плода и формирование определенного ВПР ОМС. Течение беременности имеет большое влияние на развитие плода. Условия гипоксии и недостаточного питания создаются для зародыша при кровотечениях, угрожающих выкидышах, резко выраженных токсикозах беременности. При анализе течения беременности у женщин, дети которых были включены в данное исследование, обнаружена тенденция к увеличению процента осложнений беременности при наличии у плода врожденной патологии почек (р<0,05). О безопасности лекарственных препаратов при беременности известно очень мало. В силу этических причин рандомизированные исследования с участием беременных проводятся крайне редко, а в широкой практике врачи, назначая лекарства, не прослеживают исходы беременности. Большинство матерей включенных в исследование детей не применяли никаких лекарств во время беременности. Так, в контрольной группе 34 женщины сообщили об отсутствии приема лекарственных препаратов во время беременности, в то время как у матерей, дети которых страдали ПМР и гидронефрозом, отмечался более высокий процент приема лекарственных препаратов (р<0,05 по сравнению с контрольной группой). Из лекарственных препаратов наиболее часто использовались гормональные препараты (20%, 10% и 5%, соответственно по группам), диуретики (6%, 7,5% и 2%, соответственно), жаропонижающие препараты (8%, 10% и 5% в первой, второй и контрольной группах, соответственно), а также антибиотики (8%, 7,5% и 2,5% в I, II и контрольной группах, соответственно). При анализе соматической патологии, было выявлено, что матери детей с ПМР и гидронефрозом статистически значимо чаще болели острыми респираторными вирусными инфекциями (ОРВИ) в первом триместре беременности (34% и 30% соответственно) (табл. 2).
Таблица 2. Факторы риска во время беременности развития пороков органов мочевой системы
Родоразрешение на сроке от 38 до 42 недели отмечалось у 34 (68%) женщин в группе I, 30 (75%) женщин в группе II и у 36 (90%) женщин в контрольной группе, что говорит о более высокой распространенности преждевременных и запоздалых родов при наличии почечной патологии у плода, что также согласуется с более высокой распространенностью осложнений беременности в указанных группах. Таким образом, в ходе проведенного исследования была выявлена мультифакторная природа возникновения пороков ОМС. При многофакторном анализе социальных биологических факторов установлено, что ведущими ФР формирования заболеваний ОМС у детей являются наличие заболеваний почек в семье, особенно у матери; отягощенный антенатальный период и акушерский анамнез у матери (осложненное течение беременности, предшествующие выкидыши и др.); профессиональные вредности, прием медикаментов. Частота тератогенных воздействий, в том числе влияния лекарственных средств, профессиональных вредностей, инфекционных заболеваний (ОРВИ) в период беременности у матерей детей с пороками развития ОМС была статистически значимо выше, чем у матерей детей контрольной группы (р<0,05). Женщинам, имеющим по роду своей работы контакт с активными химическими факторами и солями тяжелых металлов, следует планировать беременность. За 2-3 месяца до зачатия и весь период беременности (особенно в сроки до 14-16 недель) желательно исключить контакт с химическими веществами, которые могут вызвать тератогенный эффект у плода. Назначать лекарственные средства беременным необходимо по строгим показаниям, лишь в случае, если ожидаемая польза превышает возможный риск для плода, используя лекарственные средства (ЛС) с установленной безопасностью и длительным опытом применения у беременных, причем в минимальных эффективных дозах. Также необходим регулярный мониторинг применения ЛС во время беременности и соответствия лекарственной терапии рекомендациям, основанным на данных доказательной медицины с целью повышения ее качества и безопасности, а также избегания возникновения пороков развития ОМС.
Выводы. Женщинам группы риска требуется проведение целенаправленного обследования, рациональной тактики ведения беременности, своевременного выявления ВПР плода. Важными составляющими оздоровительных мероприятий являются: соответствующая подготовка девушек фертильного возраста, недопущение воздействия вредных факторов на плод, тщательный сбор анамнеза, эффективное наблюдение и лечение на поликлиническом этапе.