Особенности развития и течения инфекции мочевых путей у больных сахарным диабетом
| Сергей Анатольевич Дубский К.м.н., врач-уролог отделения андрологии и урологии ФГУ «Эндокринологический научный центр» Минздравсоцразвития [email protected] |
| Александр Евгеньевич Лепетухин К.м.н., врач-уролог отделения андрологии и урологии ФГУ «Эндокринологический научный центр» Минздравсоцразвития [email protected] |
Нарушение углеводного обмена оказывает негативное влияние практически на все органы и системы человеческого организма, в том числе и на мочеполовую систему. Среди основных урологических осложнений при сахарном диабете (СД) наиболее часто встречаются инфекции мочевых путей (ИМП). Один из специфических процессов при СД повышение концентрации глюкозы в моче на фоне гипергликемии, что служит фактором риска повреждения уротелия, его серозно-мукоидного слоя.
Основными патогенетическими факторами, обусловливающими развитие ИМП и воспалительных заболеваний мочеполовой системы при СД, являются:
- токсическое и дисметаболическое воздействие гипергликемии;
- микрои макроангиопатии, способствующие ишемии тканей мочеполовой системы;
- специфическая полинейропатия, приводящая к нейрогенной дисфункции мышечного слоя с дальнейшим развитием ретенции мочи;
- сниженная фагоцитарная активность лейкоцитов и бактерицидность мочи на фоне гиперглюкозурии.
При СД 1 типа к вышеперечисленным факторам относят длительное течение СД, дебют СД до и в период полового созревания с ранним (через 5-10 лет) развитием периферической и автономной нейропатии.
Важным фактором защиты макроорганизма от инфекции является уровень половых гормонов, в частности: уровень эстрогена и прогестерона — для женщин и тестостерона — для мужчин. Различные исследования показали наличие в уретре большого количества рецепторов к эстрогенам. Образование серозно-мукоидного слоя на поверхности уротелия считается гормонально-зависимым процессом: эстрогены влияют на синтез мукополисахаридов, а прогестерон — на их выделение эпителиальными клетками. Подтверждается также и положительная роль тестостерона в воздействии на рецепторы уротелия.
Особенности диагностики и лечения острых и хронических воспалительных заболеваний почек у больных СД
Длительная декомпенсация углеводного обмена служит фактором риска развития и прогрессирования острого инфекционновоспалительного процесса в почках, однако сам пиелонефрит не является осложнением СД. Установлено, что больные СД особенно уязвимы для быстрого прогрессирования инфекции в почечной паренхиме и ее последующих осложнений. В свою очередь острый пиелонефрит (ОП) и хроническое воспаление в почках это факторы, усугубляющие течение такого грозного специфического осложнения как диабетическая нефропатия. Склонность к катаболическим процессам и отчетливое снижение микроциркуляции ухудшают течение гнойной инфекции в почках.
Дополнительным фактором, усугубляющим развитие ОП и прогрессирование хронического пиелонефрита, является эндотелиальная дисфункция, которая на фоне длительного воздействия гипергликемии приводит к нарушению ангиогенеза и гемостаза. Прямое глюкозотоксичное влияние приводит к снижению синтеза NO и повышению концентрации эндотелина-1 в почечных сосудах, что в результате вызывает их констрикцию, агрегации тромбоцитов, адгезии монои тромбоцитов.
Применение ультразвукового (УЗИ) допплерографического исследования и мультиспиральной компьютерной томографии (МСКТ) в диагностике ОП позволяет оценивать глубину и степень деструкции, дифференцировать диффузное поражение от фокального, а также регистрировать распространение воспалительного процесса в ретроперитонеальную область. Допплерографическое исследование в диагностике ОП дает информацию о структурно-функциональном состоянии кровотока в почках и эласто-тонических свойствах сосудов. Так, УЗИ и допплерографическое исследование почек при декомпенсации СД может выполняться до 2 раз в день. Выполнение МСКТ с контрастированием требует обязательного использования только низкоосмолярных растворов, достаточной гидратации и контроля над функцией почек (уровень креатинина крови) в течение ближайших 3 дней для исключения контрастиндуцированной нефропатии.
Назначение антибактериальной терапии пациентам с СД и ОП следует проводить одновременно со стабилизацией гликемии, уровень которой следует приблизить к предполагаемым индивидуальным целевым значениям. Пациентов с СД 2 типа при тяжелом течении ОП, находящихся в режиме диетотерапии или принимающих пероральные сахароснижающие препараты, следует незамедлительно перевести на инсулинотерапию и в дальнейшем, до разрешения ситуации, вести как хирургических больных.
Антибактериальная терапия ОП при сохранном или восстановленном пассаже мочи должна начинаться без промедления. Согласно рекомендациям Европейской ассоциации урологов (2010) по лечению ИМП, у пациентов с осложненным пиелонефритом рекомендуется терапия фторхинолонами, аминопенициллинами с ингибиторами р-лактамаз, цефалоспоринами П-Ш поколения (например, Супракс — пероральный цефалоспорин III поколения), карбопенемами и аминогликозидами. Однако известно, что применение аминогликозидов у пациентов с СД, в связи с их выраженной нефротоксичностью, возможно только в исключительных случаях и под тщательным контролем функции почек.
Согласно мнению отечественных и зарубежных специалистов ОП следует рассматривать как острое хирургическое заболевание, при котором в случаях развития гнойного процесса больные подлежат оперативному вмешательству. В то же время в литературе имеются сообщения, что в некоторых случаях даже гнойные формы ОП у больных СД можно успешно лечить консервативными методами при условии своевременной диагностики, сохраненном пассаже мочи и раннем начале терапии. При дальнейшем наблюдении данной группы пациентов, получавших консервативную терапию ОП, по данным лучевых методов исследования, участков нефросклероза не отмечается.
Наиболее часто выявляемым возбудителем ИМП как у пациентов с СД, так и без него, является E. coli. Также часто причиной инфицирования могут быть Enterobacteriaceae и Klebsiella. Хотя основные возбудители пиелонефрита при СД бактерии, определенная роль принадлежит и грибам. При развитии пиелонефрита на фоне СД имеется высокий риск развития кандидоза мочевой системы с преобладанием Candida alb. Патогенные свойства Candida alb, обусловливающие поражение различных органов, включая мочевые пути, проявляются только при существенном ослаблении иммунологической защиты.
При лечении кандидозной инфекции у больных СД необходимо учитывать следующие особенности:
- предпочтителен противогрибковый препарат с наименьшим уровнем побочных действий (флуконазол Микосист); он угнетает деятельность ферментов, увеличивая тем самым проницаемость клеточной мембраны и нарушая рост и размножение грибов;
- при длительном хроническом течении заболевания и, как правило, вялотекущем процессе, требуется применять продолжительную схему лечения;
- после проведения основного курса лечения больной должен оставаться на диспансерном учете.
Инфекция нижних мочевых путей и половых органов
Мужчины с СД на фоне специфической полинейропатии могут иметь бессимптомное течение хронического простатита. Вследствие этого, осмотр урологом необходим ежегодно или в случае необъяснимого ухудшения контроля гликемии. При наличии увеличенного числа лейкоцитов в секрете предстательной железы у больных СД, даже при отсутствии симптомов воспаления необходимо исследование стерильности секрета простаты и определение антибиотикочувствительности. Основным критерием диагностики и результатов лечения больных хроническим простатитом должны быть динамика симптомов и лабораторных показателей, которые в свою очередь должны оцениваться совместно с компенсацией углеводного обмена.
Важную роль в развитии инфекций нижних мочевых путей (ИНМП) у женщин с СД играет гипоксия детрузора и повреждение уротелия, которые усиливаются на фоне длительной декомпенсации углеводного обмена. Также большое значение имеет эстрогенный дефицит, который в свою очередь может формироваться на фоне хронической гипергликемии. Дефицит эстрогенов дополнительно приводит к апоптозу гладкомышечных волокон, повреждению проводящих нервных волокон, ультраструктурным изменениям в детрузоре, уротелии, серозно-мукоидном защитном поверхностном слое. Именно поэтому кроме стандартных урологических исследований при подозрении на ИМП, необходимо провести диагностический поиск возможного дефицита половых гормонов. Назначение заместительной гормональной терапии у пациенток с СД и нарушением уровня эстрогенов имеет положительный результат.
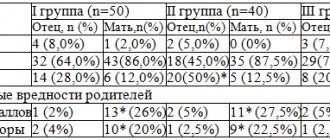
Асимптоматическая бактериурия (АБ) является частым состоянием у мужчин и женщин с СД. В проведенных исследованиях АБ более 105 КОЕ/мл у женщин и мужчин с СД определяется в 9,0-27 % и 0,7-11 % случаев соответственно. У 70 % женщин с СД и АБ определяется лейкоцитурия. Согласно данным зарубежных исследований, пиурия на фоне АБ не требует проведения антибактериальной терапии. Также доказано, что АБ у пациентов с СД не является показанием к проведению антибактериальной терапии.
Терапия ИНМП у больных СД проводится по тем же принципам, что и у больных без СД, и включает в себя применение антибактериальных, антимикотических, противовоспалительных препаратов, а результат в основном зависит от уровня гликемии на момент развившегося патологического процесса и степени компенсации углеводного обмена с дебюта СД. Препаратами выбора являются фторхинолоны, аминопенициллины с ингибиторами Р-лактамаз, цефалоспорины II-III поколения (например, Супракс).
Диабетическая автономная нейропатия мочевого пузыря
Одним из важных факторов риска развития ИНМП у пациентов с СД служит автономная диабетическая нейропатия с поражением мочевого пузыря — диабетическая цистопатия (ДЦ). ДЦ характеризуется нарушением ощущения наполнения мочевого пузыря, а при прогрессировании патологических процессов — снижением сократимости детрузора, вплоть до развития хронической задержки мочи.
На сегодняшний день представления о патогенезе развития автономной нейропатии мочевого пузыря при СД сходны с развитием автономной полинейропатии других органов и систем, однако в последнее время много внимания уделяется поражению эндоневрального кровотока. Точных данных по распространенности ДЦ в мировой литературе нет. Сложность изучения данной проблемы связана с бессимптомным началом, длительным течением, а также недостатком точных рутинных методов диагностики.
В настоящее время не разработано стандартов диагностики и лечения диабетической автономной нейропатии. Предупреждение данного состояния основывается на общих принципах ведения пациентов с СД — длительная, стабильная компенсация СД с профилактикой развития микрои макроангиопатий. Диагностические мероприятия при нарушениях мочеиспускания у пациентов с СД общеизвестны:
- общеклинический анализ мочи;
- определение объема остаточной мочи;
- урофлоуметрия.
Дополнительными, уточняющими исследованиями могут быть:
- комплексное уродинамическое исследование (исследование давление/поток с электромиографией, регистрация профиля уретрального давления);
- уретроцистоскопия.
До настоящего времени не предложено метода лечения, который был бы достоверно эффективным в терапии автономной диабетической полинейропатии, в структуре которой и развивается ДЦ.
Наиболее часто рекомендуемым препаратом для лечения диабетической нейропатии является а-липоевая (тиоктовая) кислота, блокаторы фосфодиэстеразы 5 типа. Однако данные препараты могут быть эффективны только на ранних стадиях развития полинейропатии. ДЦ может быть осложнена развитием инфравезикальной обструкции, для коррекции которой используют а1-адреноблокаторы (например, Сонизин), но при их применении на фоне уже имеющейся автономной нейропатии у мужчин может развиться ретроградная эякуляция. При выраженной ДЦ рекомендуется предпринимать попытки осуществить акт мочеиспускания каждые 2-4 часа, независимо от наличия позыва на мочеиспускание и/или решать вопрос об интермиттирующей аутокатетеризации.
Таким образом, с целью профилактики инфекционно-воспалительных заболеваний почек скрининг ИМП при СД должен проводиться ежегодно. Особое внимание должно быть уделено исследованию этиопатогенетических механизмов развития инфекционновоспалительных заболеваний мочеполовых органов и мочевыводящих путей у больных СД, с разработкой новых профилактических и лечебных алгоритмов, что, безусловно, позволит не только продлить жизнь пациенту с СД, но и значительно повысить ее качество.
0
Ваша оценка: Нет
Что такое бессимптомная лейкоцитурия?
Это состояние, при котором пациент не отмечает наличие симптомов ИМП у себя, однако общий анализ мочи показывает наличие лейкоцитов в моче. При посеве мочи виновники инфекции также растут в большом количестве. 27% больных диабетом имеют бессимптомную лейкоцитурию.
Проведённые исследования показывают что бессимптомная бактериурия не снижает риск развития диабетической нефропатии при хорошо контролируемом сахарном диабете. Однако, лечить это состояние не рекомендуется, поскольку употребление антибактериальных препаратов приводит к повышению устойчивости бактерий к лечению. Это может привести к развитию более тяжёлых форм ИМП в будущем.
Инструментальные методы диагностики
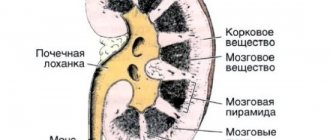
Ультразвуковое исследование (УЗИ) у больных пиелонефритом может выявить характерные изменения структуры почечной ткани: расширение почечной лоханки, огрубение контура чашечек, неоднородность паренхимы с участками ее рубцевания (при длительном анамнезе заболевания). Кроме того, УЗИ — ценный метод диагностики состояний, являющихся причиной пиелонефрита или поддерживающих егохроническое течение — гидронефроз вследствие нейрогенного мочевого пузыря, уролитиаз, поликистоз почек. Рентгенологические методы в диагностике пиелонефрита в настоящее время отодвинуты на вторые позиции в силу опасности лучевой нагрузки, необходимости введения рентгеноконтрастных веществ, что небезопасно у больных СД. Компьютерная томография почек не имеет существенных преимуществ перед УЗИ, используется для дифференциации с опухолевыми процессами. Радионуклидные методы диагностики используют для определения массы функционирующей паренхимы, что имеет прогностическое значение.
Лечение
Первым шагом в лечении полинейропатии является поддержание глюкозы крови в целевом диапазоне, согласованным врачом, и снижение высокого артериального давления и уровня холестерина.
Управление уровнем глюкозы сведет к минимуму риск диабетической нейропатии. Ключевой частью лечения является уменьшение боли и устранение некоторых симптомов.
Некоторые лекарственные препараты и физиотерапия могут помочь контролировать боль при диабетической нейропатии, наряду с другими методами лечения. Однако они не могут восстановить нервные клетки. Пациенты также должны бросить курить и ограничить потребление алкоголя максимум одной дозой в день для женщин и двумя для мужчин.
Типы
Периферическая нейропатия может привести к потере чувствительности в ногах.
Выделяют четыре основных типа нейропатии:
- Периферическая симметричная нейропатия: влияет на стопы и руки. Это самая распространенная форма диабетической нейропатии.
- Автономная нейропатия: развивается в нервных волокнах, которые контролируют непроизвольные функции организма, такие как пищеварение, мочеиспускание или сердечный ритм.
- Проксимальная нейропатия: поражает нервы, корешки, сплетения определенного отдела позвоночника
- Мононейропатии: поражается любой нерв.
Симптомы нейропатии зависят от типа и пораженного нерва.
Лекарственные препараты
Выделяют ряд препаратов, которые могут помочь справиться с болью:
- противосудорожные препараты
- трициклические антидепрессанты
- опиоиды и неопиоидные обезболивающие препараты
Употребление опиоидов может привести к зависимости, поэтому врачи должны назначать их как можно в меньшей дозе
Физиотерапия, применяемая в сочетании с медикаментами, может помочь облегчить боль и снизить риск зависимости от опиоидов.
Мануальный терапевт, массажист или остеопат может проводить регулярные массажи или мануальную терапию для растяжения мышц. Массаж может подавлять мышечные сокращения, судороги и атрофию из-за плохого кровоснабжения.
Специальные упражнения, такие как плавание или аэробика, могут помочь человеку развить и поддержать мышечную силу и уменьшить потерю мышечной массы.
Терапевтический ультразвук — это еще один вид физиотерапии, в котором ультразвуковые волны для стимуляции ткани под кожей. Это может помочь некоторым людям восстановить чувствительность в ногах.