ДИАГНОСТИКА И ПРИНЦИПЫ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ
The communication presents current diagnostic methods in chronic renal failure (CRF), outlines principles of its treatment. Great emphasis is laid on the importance of early medical treatment of CRF, whose main components are low-protein diets and hypertension control. The paper lists indications for dialysis, outlines principles of choice of its procedure, describes approaches to treating and preventing dyalisis-induced complications.
А.Ю.Николаев, Н.Л.Лифшиц,Ю.С.Милованов Проблемная лаборатория нефрологии (зав.- член-корр.РАМН И.Е.Тареева) ММА им. И.М.Сеченова A.Yu.Nikolayev, N.L.Lifshits, Yu.S.Milovanov Task Force Laboratory of Nephrology, (Head is I.Ye.Tareyeva, Corresponding Member of the Russian Academy of Medical Sciences), I.M.Sechenov Moscow Medical Academy
Х
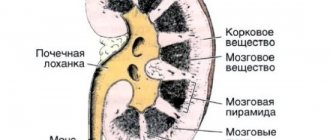
роническая почечная недостаточность (ХПН) – симптомокомплекс, вызванный необратимой постепенной гибелью нефронов вследствие первичного или вторичного хронического прогрессирующего заболевания почек.
Распространенность и причины ХПН
Частота ХПН колеблется в различных странах (в пределах 100-600 на 1 млн взрослого населения) и увеличивается с возрастом. Если у детей к ХПН приводят преимущественно врожденные и наследственные нефропатии, то у взрослых — брайтов гломерулонефрит, хронический пиелонефрит. В пожилом и старческом возрасте среди причин ХПН наиболее важную роль играют сахарный диабет, подагра, гипертоническая болезнь, атеросклероз, обструктивные урологические и онкологические заболевания, лекарственные поражения почек. Так, среди больных ХПН, находящихся на хроническом диализном лечении в США и Западной Европе, 20-25% составляют больные диабетической нефропатией. В странах Африки и Азии среди главных причин ХПН фигурируют малярийная, шистосомная нефропатии и ВИЧ-нефропатия.
Клинические проявления ХПН
У больного ХПН раньше других симптомов отмечаются жалобы на снижение аппетита, сухость и неприятный вкус во рту, тошноту, тяжесть в эпигастрии. Типичны полиурия, никтурия, утомляемость, зябкость, инверсия сна, кожный зуд, тонические судороги икроножных мышц. При тяжелом гипертоническом синдроме нередко присоединяются головная боль, осложнения со стороны сердца, сосудов мозга и глазного дна со снижением зрения, вплоть до полной слепоты. При осмотре обращает на себя внимание своеобразная желтоватая бледность кожных покровов. Кожа сухая (больные не потеют), тургор ее снижен, отмечаются геморрагии и следы расчесов. Артериальное давление (АД), как правило, повышено. Общая мышечная масса часто снижена. Характерны частые носовые кровотечения, одутловатость лица, уринозный запах изо рта (при далеко зашедшей уремии). Больные вялы, апатичны, медлительны в движениях и ответах на вопросы. В терминальной стадии уремии развиваются тяжелая гипергидратация (анасарка, интерстициальный отек легких, острая левожелудочковая недостаточность, отек мозга), декомпенсированный метаболический ацидоз (периодическое дыхание Куссмауля), критическая гиперкалиемия, перикардит, сопорозное состояние, переходящее в уремическую кому.
Диагностика ХПН
Ранняя диагностика ХПН нередко вызывает трудности. С одной стороны, нередко наблюдается многолетнее бессимптомное течение ХПН, особенно характерное для хронического пиелонефрита, латентного нефрита, поликистозной болезни. С другой стороны, в связи с полиморфизмом поражений внутренних органов при далеко зашедшей ХПН на первый план могут выходить ее неспецифические «маски»: анемическая, гипертоническая, астеническая, подагрическая, остеопатическая. Наличие у больного стойкой нормохромной анемии в сочетании с полиурией и артериальной гипертонией должно настораживать в отношении ХПН. Однако ранняя диагностика ХПН основана преимущественно на лабораторных и биохимических методах. Информативно и надежно определение максимальной относительной плотности (осмолярности) мочи, величины клубочковой фильтрации (КФ) и уровня креатинина (Кр) в сыворотке крови. Уменьшение максимальной относительной плотности мочи ниже 1018 в пробе Зимницкого наряду со снижением КФ в пробе Реберга до уровня менее 60 мл/мин свидетельствует о начальной стадии ХПН. Азотемия (Кр>0,12 ммоль/л) присоединяется на более поздней стадии – при снижении КФ до 40 – 30 мл/мин. В пользу ХПН в плане ее разграничения с острой почечной недостаточностью говорят данные длительного «почечного анамнеза», нарушения фосфорно-кальциевого обмена, а также уменьшение размеров почек. В зависимости от стадии ХПН применяется консервативное и активное лечение.
Консервативное лечение ХПН
Задачи консервативной терапии заключаются в замедлении темпов прогрессирования ХПН, в устранении факторов, усугубляющих ее течение (интеркуррентные инфекции, водно-электролитные нарушения, гиповолемия, нефротоксичность медикаментов), а также в коррекции свойственных уремии гормональных и метаболических нарушений (анемия, гиперфосфатемия, гиперлипидемия). Особенно важное значение имеют соблюдение малобелковой диеты (МБД) и контроль за почечной гипертонией. Соблюдение МБД уменьшает выраженность азотемии, улучшает показатели фосфорно-кальциевого обмена, способствует более длительному сохранению остаточной функции почек. В начальной стадии ХПН потребление белка ограничивается до 0,7 – 0,8 г на 1 кг массы тела. При более выраженной ХПН (Кр крови 0,35 – 0,5 ммоль/л, мочевина 16 – 20 ммоль/л) переходят на диету 7б с ограничением белка до 0,5 г/кг в сутки, калия до 2,7 г/сут, фосфора до 700 мг/сут. При далеко зашедшей ХПН (Кр>0,5 ммоль/л, мочевина более 20 ммоль/л, КФ 10 – 25 мл/мин) рекомендуется диета 7а (типа Джиованетти) с резким ограничением белка (0,25 – 0,3 г/кг в сутки), калия (до 1,6 г/сут), фосфора (до 400 мг/сут). При этом не менее половины суточного количества белка должен составлять полноценный (творог, яйца, мясо) белок. В связи с характерными для ХПН нарушениями липидного обмена, приводящими к раннему атеросклерозу с высоким риском развития ИБС и сосудисто-мозговой патологии, полезно обогащение МБД полиненасыщенными жирными кислотами (растительное масло, морепродукты, рыбий жир). Калорийность МБД не должна быть ниже 2100 – 2200 ккал/сут, оптимально поддержание ее на уровне 3000 ккал/сут, что достигается увеличением содержания углеводов и жиров. Cочетание МБД с препаратами эссенциальных кетокислот (кетостерил , Германия и др.) снижает риск развития отрицательного азотистого баланса и улучшает утилизацию азота мочевины в организме больного. Об эффективности МБД свидетельствуют уменьшение симптомов уремической интоксикации, снижение уровня мочевины и фосфатов крови при отсутствии снижения массы тела, гипоальбуминемии, гиперкалиемии и стабильном уровне pH и сывороточных бикарбонатов. Артериальная гипертония – один из основных факторов, ускоряющих прогрессирование ХПН, — в большинстве случаев связана с задержкой натрия и воды (объем-натрийзависимая), поэтому для лечения крайне важны индивидуальные рекомендации по соблюдению водно-солевого режима, определяемые с учетом выраженности полиурии и суточной экскреции натрия с мочой. Выведение избытка натрия и жидкости достигается также назначением салуретиков (фуросемид, буметанид); c осторожностью (из-за опасности ототоксического действия) применяют этакриновую кислоту. Не рекомендуется использование у больных ХПН калийсберегающих диуретиков (верошпирона, триампура, амилорида). Тиазидовые диуретики ( гипотиазид, хлорталидон, гигротон) противопоказаны. Лечение артериальной гипертонии, которое у больных ХПН должно быть длительным и непрерывным, следует начинать с малых доз с постепенным увеличением до терапевтического уровня, так как резкое снижение АД может привести к гиповолемии и усугубить ХПН (одномоментное снижение АД от исходного уровня не должно превышать 25%). Уровень АД, при котором у больных ХПН поддерживается почечный кровоток, достаточный для максимально возможной КФ обычно на 10 – 15 мм р. ст. выше возрастной нормы. Однако в последнее время поэтому оптимальным признано является достижение нормального АД. Наиболее подходящими симпатолитиками при лечении гипертонии у больных ХПН являются допегит и клофелин, при систематическом применении хорошо сочетающиеся с салуретиками. Доза допегита в связи с замедленным его выведением должна уменьшаться в 1,5 – 2 раза. Более сильным гипотензивным действием и благоприятным влиянием на почечный кровоток характеризуются периферические артериолодилататоры (миноксидил, гидралазин), комбинируемые с салуретиками и малыми дозами бета-блокаторов. Антагонисты ионов кальция (нифедипин, никардипин, исрадипин, дилтиазем и др.), не вызывающие задержки натрия и воды, снижения почечного кровотока, не активируют РААС и поэтому могут использоваться при ХПН как для монотерапии, так и в сочетаниях. При более тяжелой ренинзависимой гипертонии больным с ХПН назначают препараты, снижающие секрецию ренина: большие дозы бета-блокаторов (обзидан 160 – 400 мг/сут, сектраль 400 – 600 мг/сут), блокатор альфа- и бета-адренорецепторов (лабеталол). При сочетании гипертонии с сердечной недостаточностью бета-блокаторы следует применять с осторожностью в сочетании с салуретиками, нитратами, сердечными гликозидами. Дозу сердечных гликозидов уменьшают с учетом особенностей фармакодинамики при ХПН и уровня калия до 50 – 70% от терапевтической. При рефрактерности к другим гипотензивным препаратам (неконтролируемой почечной гипертонии) используются ингибиторы ангиотензин-конвертирующего фермента – АКФ (каптоприл, эналаприл, рамиприл, лизиноприл), применяемые в виде монотерапии или в сочетании с салуретиками, бета-блокаторами, антагонистами кальция. Ингибиторы АКФ и некоторые антагонисты кальция (верапамил, дилтиазем) обладают нефропротективным свойством, способностью снижать внутриклубочковую гипертензию, протеинурию и значимо замедлять темп прогрессирования ХПН, в связи с чем их выделяют как препараты первого выбора у больных с ХПН, особенно при диабетической нефропатии с самых ранних стадий. В последнее время появились новые перспективные препараты из группы блокаторов тканевых рецепторов к ангиотензину II (лозартан, ирбесартан), свободные от ряда побочных действий ингибиторов АКФ. Для купирования гипертонических кризов у больных ХПН рекомендуются сублингвально клофелин, коринфар или капотен или парентеральное введение лазикса, изоптина, миноксидила или периферических вазодилататоров (диазоксида, нитропруссида натрия). Комбинация препаратов с различными механизмами антигипертензивного действия позволяет добиваться эффекта без применения высоких доз медикаментов. Рекомендуемые комбинации: ингибитор АКФ + салуретик + бета-блокатор; антагонист кальция + бета-блокатор + симпатолитик на фоне ограничения соли и т. д.
Активное лечение ХПН
В настоящее время используются три метода активного лечения уремии: хронический гемодиализ (ГД), хронический перитонеальный диализ ( ПД ) и трансплантация почки. Проблемы трансплантации почки выходят за рамки данной публикации. Гемодиализ ( ГД )
проводится путем подключения артериовенозной фистулы к монитору «искусcтвенная почка». Азотистые шлаки и электролиты диффундируют через синтетическую полупроницаемую мембрану, а вода удаляется под действием гидростатического давления со стороны крови (ультрафильтрация). Стандартный ГД выполняется в интермиттирующем режиме 2 – 3 раза в неделю (диализное время 12 – 15 ч в неделю) на ацетатном или бикарбонатном буфере.
Перитонеальный диализ (ПД)
осуществляют путем введения в брюшную полость диализирующего раствора через хронический перитонеальный катетер. При этом роль полупроницаемой мембраны, элиминирующей азотистые шлаки и электролиты, выполняет мезотелий брюшины. Удаление воды (ультрафильтрация) происходит под действием осмотического градиента давления за счет применения растворов с высокой концентрацией глюкозы (декстрозы).
Показания к началу диализного лечения ХПН
Раннему взятию на диализное лечение (при уровне Кр крови менее 0,6 – 0,7 ммоль/л, КФ более 10 – 15 мл/мин ) подлежат больные старческого и детского возраста, больные тяжелым диабетом, ИБС, больные с нефротическим синдромом, кахексией, неконтролируемой гипертонией, хроническими инфекциями, уремической полинейропатией, гипергидратацией, гиперкалиемией, декомпенсированным метаболическим ацидозом. В остальных случаях диализное лечение следует начинать в терминальной стадии ХПН ( при повышении уровня Кр более 0,7 – 0,9 ммоль/л и снижении КФ ниже 10 мл/мин) после использования всех возможностей консервативной терапии. Для успеха активного лечения уремии важны уровень психологической адаптации больного к лечению, правильный выбор диализного метода и эффективного диализного режима, переносимость буфера. Так, бикарбонатный ГД
показан при непереносимости ацетата (нарушении его метаболизма при дефиците мышечной массы, кахексии ), при тяжелом метаболическом ацидозе, сахарном диабете, артериальной гипотонии, при хронической сердечной недостаточности, обструктивных заболеваниях легких. При стандартном ГД удаление избытка воды, натрия, калия и азотистых шлаков осуществляется ускоренно во время очередного сеанса. К осложнениям такого нефизиологичного интермиттирующего режима относятся: быстрое снижение уровня мочевины и натрия в крови c развитием гипоосмолярного синдрома, уменьшение объема циркулирующей крови (ОЦК) с синдиализной гипотонией, острым нарушением коронарного и церебрального кровоснабжения, снижение уровня калия в крови с нарушениями сердечного ритма. При нестабильности гемодинамики при стандартном ГД может быть полезным «низкоскоростной» ГД с применением низкопроницаемых мембран большой площади. Сеанс такого ГД длится в 1,5 – 2 раза дольше, чем сеанс стандартного (диализное время 20 – 24 ч в неделю), что обеспечивает лучший контроль гемодинамики, ОЦК, осмотического гомеостаза. При отсутствии эффекта показаны применение бикарбонатного компьютерного ГД на высокопроницаемых мембранах (ВПМ), гемодиафильтрация или перевод на ПД. ГД на ВПМ и гемодиафильтрация построены на принципах автоматического контроля за изменениями ОЦК, осмолярности плазмы и скорости ультрафильтрации. Так, опасное снижение осмолярности плазмы, тенденция к гиповолемии, коллапсу на ГД могут корригироваться посредством увеличения концентрации натрия в диализирующем растворе ( профилированием натрия ), снижения скорости ультрафильтрации, увеличения скорости внутривенной инфузии замещающего раствора. ГД на ВПМ показан при тяжелой уремической интоксикации, анурии, гиперкатаболических состояниях, инфекционных осложнениях, кахексии, критической гипергидратации, неконтролируемой гипертонии, сердечной недостаточности, синдиализной гипотонии, гиперфосфатемии. При невозможности сформировать надежную артериовенозную фистулу лечение ХПН реально лишь с помощью ПД. Перевод на ПД целесообразен и в тех случаях, когда больной плохо переносит стандартный ГД, а ГД на ВПМ осуществить невозможно. Так, больные ХПН, страдающие тяжелой ИБС, хронической сердечной недостаточностью, артериальной гипотонией, лучше адаптируются к ПД. Наконец, носители вирусов гепатита В, С, СПИДа, больные ХПН, на ПД менее опасны для окружающих, чем вирусоносители, находящиеся на ГД. Постоянный амбулаторный перитонеальный диализ (ПАПД) нашел широкое применение в качестве домашнего диализа. При ПАПД диализирующий раствор остается в брюшной полости постоянно, его смену проводит на дому сам больной 4 – 5 раз в сутки. Процедура замены использованного раствора на свежий занимает у обученного больного 10-20 мин. При этом за сутки сменяется 7 – 9 л диализирующего раствора. Решающее условие эффективности диализного лечения –
оптимизация его дозы.
С учетом выраженности азотемии, гипергидратации, величины остаточной функции почек выбирается оптимальный режим (диализная доза): суммарный клиренс мочевины и интенсивность ультрафильтрации. При необоснованном сокращении диализного времени, несоблюдении больным водно-солевого режима, гиперкатаболизме, потере остаточной функции почек формируется крайне неблагоприятный прогностически
синдром недодиализа.
Он характеризуется сохраняющейся на фоне диализного лечения гипергидратацией (объем-натрийзависимая гипертония с застойной сердечной недостаточностью, повторный отек легких, асцит), рецидивами перикардита, прогрессирующей полинейропатией. Важно подчеркнуть, что гипертония на ГД может быть проявлением ХПН, симптомом недодиализа, осложнением лекарственной терапии и поэтому требует дифференцированного подхода к лечению. Если объем-натрийзависимая гипертония в рамках синдрома недодиализа должна корригироваться посредством увеличения диализного времени и ужесточения междиализного водно-солевого режима, то в лечении ренинзависимой, неконтролируемой ГД гипертонии важное место занимают гипотензивные средства, указанные выше, а также хирургические методы. Хирургическому лечению подлежат стеноз почечной артерии, аденома паращитовидной железы, аденокарцинома в кисте сморщенной почки. Наконец, при лекарственной гипертонии (стероидной, сандиммуновой, эритропоэтиновой) требуется уменьшение дозы или временная отмена соответствующих медикаментов.
Осложнения диализного лечения
также могут определять прогноз и качество жизни у больных ХПН. Крайне актуальна проблема инфекционных осложнений, распространенность которых объясняется уремическим иммунодефицитом и легкостью инфицирования (парентерального, интраперитонеального ) во время процедуры диализа. У 40 – 50% больных на диализе обнаруживается вирусоносительство ( HBV, HCV ) и бактерионосительство (золотистого стафилококка). Острые инфекционные осложнения приводят к смерти 15 – 20% больных на ГД и ПАПД. У больных на ГД среди самых частых инфекционных осложнений фигурирует острый вирусный гепатит ( HBV, HCV ), а наиболее опасными являются пневмонии, шунт-сепсис с острым инфекционным эндокардитом, туберкулез. Распространенность туберкулеза у больных на ГД в 7 – 10 раз выше, чем в других группах пациентов, смертность от него достигает 40%. Часто присоединяется вялотекущая грамотрицательная инфекция мочевых путей с инфицированием кист в сморщенных почках, что у ослабленных больных может привести к пионефрозу, периренальному абсцессу, уросепсису. Типичным инфекционным осложнением ПАПД является перитонит. Побочные действия лекарств (передозировка с общетоксическим и нефротоксическим действием ) наблюдаются у больных на диализе особенно часто в связи с трудностями подбора эффективной дозы в условиях резко нарушенной фармакодинамики лекарств при ХПН. При выборе антибиотика важно знать не только основной путь его выведения (почками или печенью), но и степень его потери через диализную мембрану.
Эндокринные и метаболические проявления ХПН,
которые не корригируются или не полностью контролируются эффективной диализной терапией, оказывают существенное влияние на медицинскую реабилитацию и выживаемость больных на диализе. Применяющийся комплекс гормональной заместительной терапии позволяет корригировать почечную анемию (препараты эритропоэтина), уремический гиперпаратиреоз (метаболиты витамина Dз). В то же время трактовка диализной остеопатии неоднозначна. Успешно используемые при гиперпаратиреоидной остеодистрофии препараты – метаболиты витамина D3 – противопоказаны при остеомаляции в рамках хронической интоксикации алюминием, когда требуются комплексоны (десфераль). Прогрессирующая остеоартропатия у больных диализным (b2-микроглобулиновым) амилоидозом вступает в ремиссию лишь после успешной трансплантации почки. ИБС остается одной из наиболее частых причин инвалидизации и отдаленной смертности больных на ГД. К факторам риска быстрого прогрессирования коронарного атеросклероза при ХПН наряду с гипертонией, гиперпаратиреозом, анемией и гипертрофией левого желудочка относится гиперлипидемия атерогенного типа, обнаруживаемая уже на ранней стадии ХПН. Для профилактики ИБС рекомендуются обогащение диеты полиненасыщенными жирными кислотами (омега-3, омега-6), пищевыми сорбентами холестерина, а также гиполипидемические препараты. Однако необходим индивидуальный подбор дозы статинов, фибратов, никотиновой кислоты, учитывая высокий риск побочного действия лекарств у больных ХПН. Таким образом, современный подход к лечению ХПН предполагает раннее начало консервативной терапии. В терминальную стадию уремии применяют индивидуально подобранные диализные методы в комбинации с патогенетической (заместительной) терапией, а также проводят лечение осложнений ГД и ПД.
Литература:
1. В.М. Ермоленко. Хронический гемодиализ. М., 1982. 2. С. Клар, С. Массри Современная нефрология. М., 1884. 3. И. Ледебо Ацетатный гемодиализ против бикарбонатного. Лунд, Швеция, 1990 г. 4. В.М. Ермоленко Хроническая почечная недостаточность. В кн. Нефрология под ред. И.Е. Тареевой. М., 1995, т. I, с. 322–79. 5. Лечение хронической почечной недостаточности. Под ред. С.И. Рябова. Санкт–Петербург., 1997. 6. А.Ю. Николаев, С.В. Лашутин, П.В. Клепиков Сравнение различных препаратов эритропоэтина при почечной анемии. Клин. фарм. тер. 1993, №3, с. 30–3. 7. И.Е. Тареева, А.Ю. Николаев, Н.Л. Лифшиц. Диагностика и консервативное лечение хронической почечной недостаточности. Методич. рекомендации для врачей. М., 1993. 8. А.Ю. Николаев, Н.Л. Лифшиц, В.М. Ермоленко Опыт длительного применения малобелковой диеты при ХПН. Тер. архив, 1994, №6, с. 45–51. 9. Н.Л. Лифшиц, И.М. Кутырина Особенности лечения гипертонии при хронических диффузных заболеваниях почек. Materia Medica 1995, №2, с. 39–50. 10. А.Ю. Николаев, Н.Л. Лифшиц Артериальная гипертония у больных терминальной почечной недостаточностью. Урология и нефрол., 1996, №1, с. 10–3.
Препараты, растворяющие камни:
Почки обычно начинают чистить после того, как уже очищена печень. Но люди, которые одновременно страдают мочекаменной и желчнокаменной болезнью, иногда проводят одновременное очищение печени и почек от камней. По крайней мере, им кажется, что они это делают…
Скепсис в этой ситуации обоснован: дело в том, что фитолизин и другие средства действуют в небольшой степени и совершенно не влияют на некоторые виды конкрементов. Так что, увы, провести ими очищение почек от камней удается не всегда.
А вообще, людям с уже имеющимися камнями очищение печени и почек проводить не стоит, по крайней мере, самостоятельно. Нужно попросить оценить ситуацию врача. Возможно, вам требуются вовсе не медикаменты, а другие методы: либо просто наблюдение, либо серьезные меры лечения наподобие операции.