Что такое ГЭБ?
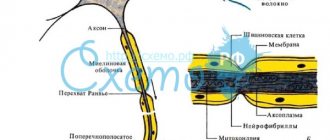
Один из самых интересных и загадочных гистогематических барьеров – это гематоэнцефалический барьер, или преграда между капиллярной кровью и нейронами центральной нервной системы. Говоря современным, информационным языком, между капиллярами и веществом головного мозга существует полностью «защищенное соединение».
Смысл гематоэнцефалического барьера (аббревиатура – ГЭБ), состоит в том, что нейроны не вступают в непосредственный контакт с капиллярной сетью, а взаимодействуют с питающими капиллярами через «посредников». Этими посредниками являются астроциты, или клетки нейроглии.
Нейроглия – это вспомогательная ткань центральной нервной системы, которая выполняет множество функций, например опорную, поддерживая нейроны, и трофическую, питая их. В данном случае, астроциты непосредственно забирают из капилляра все, что нужно нейронам, и передают им. Одновременно они контролируют, чтобы в головной мозг не попали вредные и чужеродные вещества.
Таким образом, через гематоэнцефалический барьер не проходят не только различные токсины, но и многие лекарства, и это составляет предмет исследования современной медицины, поскольку с каждым днем количество препаратов, которые регистрируются для лечения заболеваний головного мозга, а также антибактериальных и противовирусных препаратов, все увеличивается.
Немного истории
Известный врач и микробиолог, Пауль Эрлих, стал мировой знаменитостью, благодаря изобретению сальварсана, или препарата № 606, который стал первым, пусть токсичным, но эффективным препаратом для лечения застарелого сифилиса. Это лекарство содержало мышьяк.
Но Эрлих также очень много экспериментировал с красителями. Он был уверен, что точно так же, как краситель плотно пристает к ткани (индиго, пурпур, кармин), он пристанет и к болезнетворному микроорганизму, стоит только найти такое вещество. Конечно, он должен не только прочно фиксироваться на микробной клетке, но и быть смертельным для микробов. Несомненно, «подлил масла в огонь» тот факт, что он женился на дочери известного и зажиточного фабриканта – текстильщика.
И Эрлих начал экспериментировать с различными и очень ядовитыми красками: анилиновыми и трипановыми.
Вскрывая лабораторных животных, он убеждался, что краситель проникает во все органы и ткани, но не имеет возможности диффундировать (проникать) в головной мозг, который оставался бледным.
Вначале его выводы были неверными: он предположил, что просто краситель не окрашивает мозг по причине того, что в нем много жира, и он отталкивает краску.
А затем открытия, предшествующие открытию гематоэнцефалического барьера, посыпались, как из рога изобилия, и сама идея стала постепенно оформляться в умах ученых. Наибольшее значение играли следующие эксперименты:
- если ввести краситель внутривенно, то максимум, что он способен окрасить – это хориоидальные сосудистые сплетения желудочков головного мозга. Дальше ему «путь закрыт»;
- если принудительно ввести краситель в ликвор, выполнив люмбальную пункцию, то мозг окрашивался. Однако, «наружу» из ликвора краситель не попадал, и остальные ткани оставались бесцветными.
После этого совершенно логично было предположено, что ликвор – это жидкость, которая находится «по ту сторону» преграды, главная задача которой – защитить центральную нервную систему.
Впервые термин ГЭБ появился в 1900 году, сто шестнадцать лет назад. В англоязычной медицинской литературе он именуется «blood-brain barrier», а в русском языке название привилось в виде «гематоэнцефалического барьера».
В дальнейшем этот феномен изучался достаточно подробно. Перед второй мировой войной появились данные о том, что есть гематоэнцефалический и гематоликворный барьер, а также есть гематоневральный вариант, который находится не в ЦНС, а расположен в периферических нервах.
Строение и функции барьера
Именно от бесперебойной работы гематоэнцефалического барьера зависит наша жизнь. Ведь наш головной мозг потребляет пятую часть всего количества кислорода и глюкозы, и при этом его вес составляет не 20% всей массы тела, а около 2%, то есть потребление мозгом питательных веществ и кислорода в 10 раз выше среднего арифметического значения.
В отличие, например, от клеток печени, мозг работает только «на кислороде», и аэробный гликолиз — это единственный возможный вариант существования всех без исключения нейронов. В том случае, если в течение 10-12 секунд питание нейронов прекращается, то человек теряет сознание, а после остановки кровообращения, находясь в состоянии клинической смерти, шансы на полное восстановление функции мозга существуют только на протяжении 5 -6 минут.
Это время увеличивается при сильном охлаждении организма, но при нормальной температуре тела окончательная гибель мозга происходит через 8-10 минут, поэтому только интенсивная деятельность ГЭБ позволяет нам быть «в форме».
Известно, что многие неврологические заболевания развиваются только вследствие того, что нарушена проницаемость гематоэнцефалического барьера, в сторону его повышения.
Мы не будем подробно вдаваться в гистологию и биохимию структур, составляющих барьер. Отметим только лишь, что строение гематоэнцефалического барьера включает в себя особую структуру капилляров. Известны следующие особенности, приводящие к появлению барьера:
- плотные контакты между эндотелиальными клетками, выстилающими капилляры изнутри.
В других органах и тканях эндотелий капилляров выполнен «небрежно», и между клетками есть большие промежутки, через которые происходит свободный обмен тканевой жидкостью с периваскулярным пространством. Там, где капилляры формируют гематоэнцефалический барьер, клетки эндотелия расположены очень плотно, и герметичность не нарушается;
- энергетические станции – митохондрии в капиллярах превышает физиологическую потребность в таковых в других местах, поскольку гематоэнцефалический барьер требует больших затрат энергии;
- высота клеток эндотелия существенно ниже, чем в сосудах другой локализации, а количество транспортных ферментов в цитоплазме клетки значительно выше. Это позволяет отвести большую роль трансмембранному цитоплазматическому транспорту;
- эндотелий сосудов в своей глубине содержит плотную, скелетообразующую базальную мембрану, к которой снаружи прилегают отростки астроцитов;
Кроме особенностей эндотелия, снаружи от капилляров существуют особые вспомогательные клетки – перициты. Что такое перицит? Это клетка, которая может снаружи регулировать просвет капилляра, а при необходимости может обладать функциями макрофага, к захвату и уничтожению вредных клеток.
Поэтому, еще не дойдя до нейронов, мы можем отметить две линии защиты гематоэнцефалического барьера: первая – это плотные соединения эндотелиоцитов и активный транспорт, а вторая – это макрофагальная активность перицитов.
Далее гематоэнцефалический барьер включает в себя большое количество астроцитов, которые и составляют наибольшую массу этой гистогематической преграды. Это небольшие клетки, которые окружают нейроны, и, по определению их роли, умеют «почти всё».
Они постоянно обмениваются веществами с эндотелием, контролируют сохранность плотных контактов, активность перицитов и просвет капилляров. Кроме того, головному мозгу нужен холестерин, но он не может проникнуть из крови ни в ликвор, ни пройти сквозь гематоэнцефалический барьер. Поэтому астроциты берут на себя его синтез, помимо основных функций.
Кстати, одним из факторов патогенеза рассеянного склероза является нарушение миелинизации дендритов и аксонов. А для образования миелина нужен холестерин. Поэтому роль дисфункции ГЭБ в развитии демиелинизирующих заболеваний является установленной, и в последнее время изучается.
Там, где нет барьеров
А есть ли такие места в центральной нервной системе, где не существует гематоэнцефалического барьера? Казалось бы, это невозможно: столько трудов было приложено к тому, чтобы создать несколько уровней защиты от внешних вредных веществ. Но, оказывается, в некоторых местах ГЭБ не составляет единую «стену» защиты, а нем имеются отверстия. Они нужны для тех веществ, которые вырабатываются головным мозгом и отправляются на периферию в качестве команд: это гормоны гипофиза. Поэтому есть свободные участки, как раз в зоне гипофиза, и эпифиза. Они существуют, чтобы гормоны и нейротрансмиттеры могли свободно проникать в кровь.
Существует и другая зона, свободная от ГЭБ, которая находится в районе ромбовидной ямки или дна 4 желудочка головного мозга. Там находится рвотный центр. Известно, что рвота может возникать не только вследствие механического раздражения задней стенки глотки, но и при наличии токсинов, попавших в кровь. Поэтому именно в этой области и существуют особые нейроны, которые постоянно производят «мониторинг» качества крови на наличие вредных веществ.
Как только их концентрация достигнет определенной величины, эти нейроны активируются, вызывая чувство тошноты, а затем и рвоту. Справедливости ради нужно сказать, что не всегда рвота связана с концентрацией вредных веществ. Иногда, при значительном повышении внутричерепного давления (при гидроцефалии, менингитах) рвотный центр активируется вследствие прямого избыточного давления при развитии синдрома внутричерепной гипертензии. Поэтому развивается так называемая центральная, или мозговая рвота, которая может наступить внезапно, и без всяких признаков тошноты.
ГЭБ и система EphR/Ephrin: связь между нейрососудистыми и нейропсихиатрическими расстройствами
Структурная целостность гематоэнцефалического барьера (ГЭБ) необходима для создания и поддержания гомеостаза головного мозга. Любое нарушение структурных компонентов ГЭБ может оказать разрушительное воздействие на психическое здоровье. За последние пару лет было опубликована череда важных исследований нейрососудистых единиц (НСЕ). Они рассматривают ГЭБ в качестве потенциальной новой цели для разработки альтернативных методов лечения мозговых и сосудистых патологий.
Структурные компоненты и функции ГЭБ
ГЭБ представляет собой клеточно-сосудистую структуру, отделяющую центральную нервную систему от периферического кровообращения (Obermeier et al., 2013). Он состоит из цереброваскулярных эндотелиальных клеток (ЭК), образующих мозговые сосуды, частей астроцитов и внеклеточного матрикса (ВM), обеспечивающих структурную поддержку (Abbott et al., 2006). Перициты также имеют отношение к формированию ГЭБ (Cabezas et al., 2014). Все эти элементы выполняют свои функции, формируя селективный физический (Abbott et al., 2006), транспортный (Begley and Brightman, 2003) и метаболический (Pardridge, 2003, 2016) барьер, который четко контролирует прохождение молекул в и из паренхимы головного мозга и предотвращает проникновение в мозг токсинов или патогенов (Obermeier et al., 2013).
Рисунок 1. Клеточные и сигнальные компоненты гематоэнцефалического барьера (ГЭБ) в норме. Сигнальные молекулы из астроцитов, влияют на создание и/или поддержание свойств ГЭБ. Кроме того, различные представители семейства эфринов (лигандов Eph-рецепторов—Ephrins) классов «А» и «В», расположенные на астроцитах и/или перицитах, активируют рецепторы EphA и EphB на эндотелиальных клетках (ЭК), чтобы влиять на дифференцировку ЭК во время ангиогенеза и на развитие плотных контактов во время формирования барьера (барьергенеза).
Эндотелиальные клетки
Церебральные ЭК имеют уникальные характеристики по сравнению с периферическими ЭК: клетки связаны друг с другом непрерывными внутриклеточными мультипротеиновыми комплексами, называемыми плотными контактами (рис. 1). Они ограничивают ток межклеточных веществ и направляют молекулы через ГЭБ по контролируемому пути (Abbott et al., 2006). Такой физический барьер позволяет свободно пропускать в мозг и из него только небольшие газообразные и липофильные молекулы, тогда как большие молекулы должны активно переноситься посредством специальных транспортных систем, таких как глюкозный транспортёр типа 1 (GLUT-1) или транспортер больших нейтральных аминокислот типа 1 (LAT-1) (Borst and Schinkel, 2013). Потенциально вредные соединения, такие как глутамат, активно выходят из мозга даже против градиента концентрации, что требует АТФ в качестве источника энергии (Hawkins and Viña, 2016). Как правило, большие гидрофильные молекулы не могут переноситься через ГЭБ, за исключением случаев специфического рецепторного или адсорбционно-опосредованного трансцитоза (Pardridge, 2003, 2021, Strazielle и Ghersi-Egea, 2016).
Плотные контакты являются ключевыми регуляторами межклеточной проницаемости. Основными составляющими плотных контактов являются межмембранные молекулы, такие как окклюдины (Yu et al., 2005), которые связываются с цитоскелетом через вспомогательные белки, клаудины (Piehl et al., 2010) и соединительные молекулы адгезии (junctional adhesion molecules – JAM-A, -B, -C, Mandel et al., 2012). Во время раннего эмбриогенеза уже происходит прорастание сосудов, активно идет ангиогенез (Obermeier et al., 2013). Зрелые плотные каналы фиксированы и должны поддерживаться на протяжении всей жизни.
Астроциты
Астроциты через свои отростки, которыми они контактируют с сосудами мозга, регулируют свойства ГЭБ (Kettenmann and Verrratsky, 2008). Среди других функций регулирование ионного баланса вокруг ГЭБ, секреция и переработка нейротрофических факторов, необходимых для контроля плотных контактов (Gee and Keller, 2005). В частности, астроциты секретируют такие молекулы, как глиальный нейротрофический фактор (GDNF, Igarashi et al., 1999), трансформирующий ростовой фактор β (TGF-β; Dobolyi et al., 2012), ангиопоэтин 1 (ANG1, Easton, 2012), фактор роста фибробластов 2 (FGF2, Reuss и др., 2003) и сосудистый эндотелиальный фактор роста (VEGF; Rosenstein et al., 2010), который действует на ЭК, чтобы либо способствовать образованию плотных контактов, либо регулировать проницаемость ГЭБ (рисунок 1).
Менингеальные кровеносные сосуды, которые не имеют контактов с астроцитами, проявляют более высокую проницаемость сосудов, чем в случае с эндотелиальными клетками ГЭБ, что подтверждает необходимость астроцитов для индуцирования свойств ГЭБ (Lécuyer et al., 2016).
Базальная мембрана
Неклеточный компонент НСЕ представляет собой основную мембрану, состоящую из структурных белков, таких как коллаген-IV, ламинин и фибронектин (Cardoso et al., 2010). Основная функция базальной мембраны заключается в обеспечении стабильности других структур НСЕ и регулировании их взаимодействия (Baeten and Akassoglou, 2011).
Рецепторы эритропоэтин-продуцирующей гепатоцеллюлярной карциномы (EphR) и лиганды, взаимодействующие с Eph-рецепторами (эфрины — ephrin).
В 1990 году впервые была обнаружена система эритропоэтин-продуцирующая гепатоцеллюлярная карцинома (EphR)/ephrin. EphrinA1 был охарактеризован как индуцируемый фактором некроза опухоли (TNF) белок в эндотелиальных клетках пупочной вены человека (HUVEC; Holzman et al., 1990). EphRs/ephrins обычно регулирует контактную зависимость между клетками, определяя их взаимодействие. Во время развития организма эта система играет важную роль в пространственной организации, направлении аксонов, формировании синаптических связей и ремоделировании кровеносных сосудов. В зрелом возрасте система главным образом регулирует синаптическое ремоделирование, эпителиальную дифференцировку, ремоделирование костных структур, иммунную функцию, секрецию инсулина и самообновление стволовых клеток (Kullander and Klein, 2002; Yamaguchi and Pasquale, 2004; Pasquale, 2005, 2008).
Eph-рецепторы содержат наибольшее семейство рецепторных тирозинкиназ (RTK). Eph-рецепторы и эфрины можно разделить на подклассы A и B. У людей известны девять EphA и пять EphB-рецепторов. Они состоят из внеклеточной части, включающей глобулярный лигандсвязывающий домен и цитоплазматический домен. Также эфрины можно отличить по их мембранному прикреплению: эфрины А закреплены с помощью гликозилфосфатидилинозитола (GPI), тогда как Эфрины B присоединены через один трансмембранный домен, содержащий короткую цитоплазматическую PDZ-связывающую часть (Lisabeth et al., 2013).
Система EphR/Ephrin: сигнальные механизмы
Помимо известной двунаправленной сигнализации, активирующейся при взаимодействии между клетками (Pasquale, 2008; Murai and Pasquale, 2011; Klein, 2012; Lisabeth et al., 2013), имеется несколько альтернативных сигнальных механизмов с помощью системы EphR/ephrin.
При взаимодействии рецептор/лигандом активируются несколько нисходящих сигнальных каскадов опосредующих клеточное притягивание-адгезию или отталкивание в зависимости от типа и обилия лигандов и рецепторов, присутствующих на поверхностях клеток (Janes et al., 2012). Среди прочих, эти сигнальные пути включают Src-семейство киназ, митоген-активированную протеинкиназу и опосредованные интегрины (Lackmann and Boyd, 2008; Pasquale, 2008; Pitulescu and Adams, 2010). После первоначального взаимодействия рецептор/лиганд интактные комплексы EphR/ Ephrin вместе с потенциально связанными цитоплазматическими белками и окружающей мембраной имплантируются в клетки. Этот механизм называется трансэндоцитозом. Он обеспечивает механизм переключения между клеточным притягиванием-адгезией/отталкиванием и прекращением действия сигнальной активности рецепторов (Lisabeth et al., 2013).
Помимо трансэндоцитоза другой альтернативный сигнальный механизм представляет активация ферментов, которые инициируют протеолитическое расщепление (Atapattu et al., 2014). Среди таких ферментов расщепления дезинтегрин А и металлопротеазы (A disintegrin and metalloproteases – АДАМ), а также и матриксные металлопротеазы (MMP) (Atapattu et al., 2014).
Несколько EphR/ephrins обоих подклассов A и B могут взаимодействовать с ADAM, что приводит к их собственному расщеплению. Расщепление рецептора, связанного с лигандом, приводит к разрушению молекулярных связей между взаимодействующими клетками.
MMP расщепляют белки, расположенные либо на мембранах, либо во внеклеточном пространстве (Miller et al., 2008). Их основная функция – разрушить структурные компоненты эндотелиальных клеток для облегчения миграции клеток (Streuli, 1999), особенно во время ангиогенеза и воспалительных процессов (Kessenbrock et al., 2010; Palmisano and Itoh, 2010). Недавно было показано, что ММР освобождают ephrinA1 и ephrinA2 от их GPI-части, что приводит к высвобождению функциональных растворимых мономеров, которые могут действовать на отдаленные Eph-рецепторы (Beauchamp and Debinski, 2012). Вслед за исходной стадией пролиферации, опосредуемой ADAM или MMP, EphRs/ephrins могут быть дополнительно обработаны внутримембранными расщепляющими протеазами, такими как γ-секретаза (Bergmans and De Strooper, 2010) или нейропсин (Attwood et al., 2011; Morohashi and Tomita, 2013). Эти взаимодействия генерируют цитоплазматические активные фрагменты (Litterst et al., 2007; Xu and Henkemeyer, 2009), которые могут, например, регулировать поведенческие реакции, такие как тревожность (Attwood et al., 2011).
Такие сигнальные механизмы системы Eph/ephrin могут играть роль в развитии патологии головного мозга, что создает возможность для выявления альтернативных целей для терапии.
Роль системы EphR/Ephrin в развитии и функционировании сосудистой сети и ГЭБ
Взаимодействие конкретных типов клеток в правильном развитии сосудистой системы и функционировании ГЭБ является важным процессом, который требует соответствующей координации во времени и пространстве. В этой координации определенную роль играет и система EphR / ephrin.
Во время ангиогенеза VEGF индуцирует экспрессию ephrinA1, которая активирует EphA2 на соседних ЭК, тем самым оказывая ангиогенные эффекты in vitro и in vivo (Cheng et al., 2002; Brantley-Sieders et al., 2004). Астроциты высвобождают VEGF во время эмбрионального развития и, следовательно, могут способствовать раннему формированию плотных контактов. При дальнейшей дифференциации ЭК и правильном формировании ГЭБ наблюдается ингибирование активности EphA2 в эндотелиальных клетках микрососудов человеческого мозга, что играет важную роль в дальнейшем усилении плотных контактов (Zhou et al., 2011;). Таким образом, регулирование доз EphA2 может лежать в основе «переключения» между ранним/ангиогенным и поздним/барьергенным эффектами EphA2 для эндотелиоцитов. Более того, предполагается, что взаимодействия между EphA2-экспрессирующими эндотелиальными клетками с экспрессирующими ephrinA1 периваскулярными астроцитами или перицитами также могут контролировать образование плотных контактов в физиологических условиях или их дисфункцию во время патогенных процессов (Lécuyer et al., 2016). Следует учесть, что избыточная экспрессия некоторых взаимодействий EphR/ephrin может влиять на целостность ГЭБ, в конечном счете влияя на гомеостаз мозга. Астроциты экспрессируют несколько членов системы EphR / ephrin (Nestor et al., 2007), которые могут иметь значение в ходе ангиогенеза и/или барригенеза. Например, правильное взаимодействие между EphA4 / ephrinA5 на ЭК и отростках астроцитов, соответственно, необходимо для развития нормальной сосудистой системы в гиппокампе взрослых мышей (Hara et al., 2010). Также показано, что сигналы EphA4 направляют рост новых мелких сосудов в ответ на глиально-зависимую стимуляцию (Goldshmit et al., 2006).
Что касается типов «В», ephrinB2 контролирует встраивание VEGF-рецептора (VEGFR) -2, что необходимо для активации этого рецептора и правильного развития эндотелиальных клеток во время ангиогенеза (Bochenek et al., 2010; Sawamiphak et al., 2010; Pitulescu и Adams, 2014). В это же время взаимодействие EphB2/ephrinB2 необходимо для правильного формирования кровеносных сосудов (Foo et al., 2006). Для развития сердечно-сосудистой системы важными являются и EphB4/ephrinB2 обусловленные сигналы для правильного определения артериальной или венозной идентичности (Wang et al., 1998; Adams et al., 1999; Gerety et al., 1999; Gale et al., 2001; Augustin and Reiss, 2003).
Дисфункция ГЭБ и система Eph/Ephrin. Есть ли связь между нейрососудистой и нейропсихиатрической патологией?
Неплотность ГЭБ является отличительной чертой нейрососудистых патологий, сопутствующих нейровоспалительным процессам (Lee et al., 2009; Abbott and Friedman, 2012). Также были показаны признаки дисфункции ГЭБ при нейропсихиатрических расстройствах, которые сопровождались повышением уровней циркулирующих провоспалительных цитокинов и TNF (Miller et al., 2009; Janelidze et al., 2011; Liu et al., 2012; Salim et al., 2012; Najjar et al., 2013). Кроме того, доклинические и клинические исследования свидетельствуют о широком диапазоне нейрососудистых и нейропсихиатрических расстройств при которых выявляется нейровоспаление (Dantzer et al., 2008; Wood, 2014; Hodes et al., 2015; Patel and Frey, 2015; Seligman and Nemeroff, 2015, Miller and Raison, 2021, Barnes et al., 2021, Menard и др., 2017). Можно предположить, что общие нейробиологические субстраты могут лежать в основе подобных заболеваний. Ввиду регуляторных функций системы EphR/ephrin во время формирования и созревания надлежащих свойств герметизации ГЭБ кажется очевидным, что эту систему можно считать центром нарушений головного мозга, связанных с дисфункцией ГЭБ.
Доклинические исследования показали, что представители системы EphR/ephrin группы «А» ( в особенности выделяется рецептор EphA2) опосредуют воспаление во время травмы, ишемии и других хронических воспалительных состояний у мышей с нейрососудистыми заболеваниями (Jellinghaus et al., 2013; Thundyil et al., 2013; Ende et al., 2014). В частности, активация рецептора EphA2 происходит после черепно-мозговой травмы и способствует развитию воспаления путем повышения проницаемости ГЭБ (Thundyil et al., 2013). Интересно, что промотор ephrinA1, самый высокоактивный лиганд для EphA2, является мишенью провоспалительного маркера TNF (Ende et al., 2014). Кроме того, в то время как TNF обладает ангиогенными свойствами во время раннего эмбриогенеза (Cheng and Chen, 2001; Munthe and Aasheim, 2002), он также вызывает гиперпроницаемость ГЭБ у взрослых посредством активации как EphA2, так и EphA4 в эндотелиальных клетках, что сопровождается развитием или обострением нейрососудистых расстройств (Jellinghaus et al., 2013; Thundyil et al., 2013; Ende et al., 2014). Таким образом, исследование сигнальных путей, обусловленных EphA2/ephrinA1, может выявить новые молекулярные триггеры патологии с воспалительными/нейрососудистыми/нейропсихиатрическими расстройствами, что может нам указать на альтернативные цели терапевтических вмешательств. Также была показано, что связь ephrinA5, экспрессируемого на астроцитах, с его соответствующим рецептором EphA4 на эндотелиоцитах, увеличивается в гиппокампе мышей с эпилепсией височной доли, свидетельствуя об увеличенном развитии мелких сосудов, что плохо влияет на гомеостаз головного мозга (Shu et al., 2016). Интересно отметить, что селективная блокада взаимодействия EphA4/epHRin ведет к ослаблению проявления болезни, что еще больше подтверждает терапевтическую значимость избирательного воздействия на систему EphR/ephrin при нейрососудистых/нейропсихических расстройствах.
Рисунок 2. Клеточные и сигнальные компоненты ГЭБ в патологических условиях. При патологии головного мозга чрезмерная активация астроцит- или перицит-зависимых эфринных сигналов может влиять на плотные контакты посредством повышения активности Eph-рецепторов с последующим повышением проницаемости ГЭБ для воспалительных факторов, циркулирующих в крови, таких как фактор некроза опухоли (TNF). Доказано, что выраженное стрессовое воздействие коррелирует с нарушением функции ГЭБ и нарушением плотных контактов, что может вызвать более выраженные проявления неврологических и нейропсихиатрических расстройств. Однако конкретные молекулярные медиаторы таких эффектов еще не определены.
Что касается представителей группы «В», было высказано предположение, что связь между TNF и EphB2 имеет отношение к индуцированию воспалительных путей (Pozniak et al., 2014). Также было показано, что EphB2 регулирует когнитивные функции и устойчивость/уязвимость к стрессовым воздействиям (Yuferov et al., 2013; Zhang et al., 2016). Среди триггеров нейропсихиатрических расстройств стресс является одним из наиболее вредных (Charney and Manji, 2004). Показано, что всего лишь 2 дня стресса провоцируют морфологические изменения в эндотелиальных клетках, которые сопровождаются дисрегуляцией экспрессии клаудина-5 и окклюдина (рис. 2). Эти изменения сопровождаются уменьшением экспрессии глиального фибриллярного кислого протеина, что указывает на дополнительное негативное воздействие на астроциты (Sántha et al., 2016). Исследование прошлого года ясно продемонстрировало пагубные последствия стресса для проницаемости ГЭБ, которые выражались увеличением его проницаемости (Menard et al., 2017).
Доказательством того, что система EphR/ephrin может представлять собой важную терапевтическую мишень для лечения нейрососудистых и нейропсихиатрических расстройств, является контролируемая реактивация EphB4/ephrinB2 при сердечно-сосудистых расстройствах, при которой улучшаются механизмы восстановления ГЭБ (Ghori et al. , 2017).
Заключение
Несмотря на то, что в нескольких исследованиях доказано, что дисфункция ГЭБ наблюдается при широком спектре психопатологий, до сих пор неизвестно, является ли нарушение ГЭБ причиной или следствием заболевания. Уже определено, что проницаемость ГЭБ увеличивается во время воспаления, что имеет положительную сторону, так как обеспечивает прохождение факторов роста или антител, которые препятствуют воспалительному процессу. С другой стороны, улучшение герметичных свойств ГЭБ поможет в периоды стресса или гипоксии (Abbott et al., 2006).
Изучение влияния системы EphR/ephrin в отдельных компонентах ГЭБ при ангиогенезе и барьергенезе, а также их действие при физиологических и патологических процессах, может открыть новые пути для понимания нейробиологических основ неврологических заболеваний. Это может помочь выявить новые терапевтические цели для создания новых типов эффективных лекарств.
Источник.
Другие статьи выпуска
| Содержание β-амилоида в плазме, церебральная атрофия и риск деменции |
| Аутоантитела против поверхностных белков нейронов при геморрагическом инсульте |