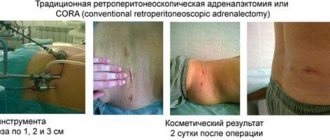
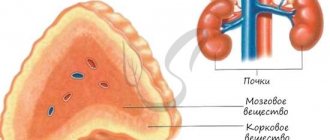
Строение и функционирование надпочечников
В основе надпочечников – две структуры:
- Мозговое вещество.
- Корковое вещество.
Они регулируются нервной системой.
Мозговое вещество
Мозговое вещество – основной источник катехоламиновых гормонов в организме — адреналина и норадреналина.
Адреналин – главный гормон при борьбе со стрессами. Увеличение его выработки происходит при положительных и негативных эмоциях, например, при травме, стрессовой ситуации.
При воздействии адреналина организм использует запасы накопленного гормона, что проявляется такими реакциями:
- резкий прилив сил;
- учащение дыхания;
- расширение зрачков.
Человек ощущает себя более сильным, чем обычно, значительно снижается болевой порог.
Норадреналин – тоже гормон стресса, но его выработка происходит перед выработкой адреналина. По воздействию намного слабее. Его функция – регуляция кровяного давления, что стимулирует работу миокарда – сердечной мышцы.
Корковое вещество
Корковое вещество надпочечников состоит из нескольких слоев, каждый из которых выполняет определенную функцию.
- Сетчатая зона.
- Пучковая зона.
- Клубочковая зона.
В сетчатой зоне синтезируются андрогены – половые гормоны. Они ответственны за развитие вторичных половых признаков и влияют на:
- состояние либидо – полового влечения у мужчин и женщин;
- уровень холестерина и липидов в крови;
- отложение жира;
- увеличение силы и массы мышц.
Независимо от пола, в каждом организме вырабатываются и мужские, и женские половые гормоны. Разница – в их количестве. Например, у женщин синтезируются эстроген и прогестерон, ответственные за репродуктивную функцию – зачатие и рождение детей, но также и тестостерон в небольшом объеме, который считается мужским гормоном.
ЛУЧЕВАЯ АНАТОМИЯ НАДПОЧЕЧНИКОВ
Лучевая анатомия человека. Под ред. Трофимовой Т.Н. 2005 год
- Нормальная анатомия и топография надпочечников
- Ультразвуковая анатомия надпочечников
- КТ-анатомия надпочечников
- МРТ-анатомия надпочечников
НОРМАЛЬНАЯ АНАТОМИЯ И ТОПОГРАФИЯ НАДПОЧЕЧНИКОВ
Надпочечник (glandulae suprarenales) — парный орган внутренней секреции, расположенный в забрюшинном пространстве над верхними полюсами почек.
Надпочечники состоят из двух морфофункционально самостоятельных эндокринных желез — мозгового и коркового вещества, имеющих различное эмбриональное происхождение [1,4].
Строение надпочечников изменяется с возрастом. У новорожденных (детей первых двух недель жизни) надпочечники имеют крупные размеры, высота их может колебаться от 23 мм до 55 мм и превышать вертикальный размер почки. Ширина надпочечника составляет 23—25 мм, толщина непосредственно после рождения может достигать 10 мм. К концу третьего года жизни надпочечники имеют минимальные размеры. Восстановление массы железы до показателей у новорожденного происходит к 5 годам.
Наиболее активный рост надпочечников отмечается в препубертатном и пубертатном периодах, в основном за счет увеличения объема коркового слоя. В это время происходит диффе-ренцировка клеток коры надпочечника с разграничением зон, свойственным взрослому человеку. У детей старшего возраста высота надпочечника может достигать 25—30 мм, а толщина не превышает 8—10 мм. После 40 лет происходит постепенное истончение сетчатой зоны, продуцирующей половые гормоны, а в климактерическом периоде почти все корковое вещество надпочечника занимает пучковая зона [4].
По форме надпочечник напоминает уплощенный в переднезаднем направлении конус со сглаженной вершиной, у которого различают три поверхности: переднюю, заднюю и нижнюю (почечную). На передней поверхности расположены ворота надпочечников. Высота надпочечников взрослого человека составляет от 25 до 45 мм, ширина — от 20 до 35 мм, толщина обычно не превышает 10 мм [5—8].
Надпочечники располагаются в забрюшинном пространстве на уровне Thx|Х|1, над верхними полюсами почек. Сзади и сверху они прилежат к поясничной части диафрагмы. Медиальнее левого надпочечника находится аорта. Спереди и кверху от него — хвост поджелудочной железы с лежащими вдоль него сосудами селезенки, а также кардиальная часть желудка. К правому надпочечнику спереди и с медиальной стороны прилежит нижняя полая вена. Передние отделы железы справа примыкают к верхнему изгибу двенадцатиперстной кишки. Латеральный отдел правого надпочечника соприкасается с висцеральной поверхностью печени. Часть передней поверхности левого надпочечника покрыта париетальной брюшиной. Вместе с почками надпочечники заключены в жировую капсулу почки.
УЛЬТРАЗВУКОВАЯ АНАТОМИЯ НАДПОЧЕЧНИКОВ
Надпочечники расположены над верхним полюсом почек и слегка смещены кпереди и медиально, имеют однородную мелкозернистую эхоструктуру. Эхогенность их превышает таковую печени, селезенки и почечной паренхимы, однако несколько ниже эхогенности срединных структур почки. Форма надпочечников может быть разнообразной и при ультразвуковом исследовании сравнивается с конусом, трапецией, усеченной пирамидой, серпом, «поварским колпаком», но всегда ассоциируется с тем или иным видом треугольника.
Размеры надпочечников вариабельны. При ультразвуковом исследовании оцениваются три размера надпочечника: ширина, высота и толщина. За ширину принимают основание «треугольника» железы, примыкающего к почке во фронтальной плоскости. Вертикальный размер (высота) измеряется по линии, перпендикулярной основанию. Толщина, или переднезадний размер, измеряется в области основания железы в сагиттальной плоскости. В среднем высота надпочечника взрослого человека при ультразвуковом исследовании составляет 18—25 мм, ширина — 16-23 мм, толщина — 12—14 мм.
Критерием правильности исследования правого надпочечника является получение на продольной сканограмме треугольника, образованного нижней полой веной, верхним полюсом правой почки и нижнезадним краем печени (рис. 12.1).
Критерием точности исследования левого надпочечника является получение на продольной сканограмме треугольника, образованного аортой, верхним полюсом левой почки и селезенкой (рис. 12.2).
Рис. 12.1. УЗИ правого надпочечника, продольное сканирование. а – схема; б — эхограмма.
1 – печень; 2 — правая почка; 3 — правый надпочечник; 4 — нижняя полая вена.
Рис. 12.2. УЗИ левого надпочечника, продольное сканирование. а — схема; б — эхограмма.
1 — селезенка; 2 — верхний полюс левой почки; 3 — левый надпочечник; 4 — аорта.
Рис. 12.3. УЗИ надпочечника новорожденного.
1 — надпочечник; 2 — правая почка; 3 — печень.
При ультразвуковом сканировании надпочечники новорожденного имеют свои особенности, которые связаны с наличием развитой фетальной зоны коркового вещества. Железы отличаются крупными размерами, сниженной эхогенностью, однородной эхоструктурой и хорошо дифференцируются на фоне гипер-эхогенной жировой клетчатки (рис. 12.3) [2].
КТ-АНАТОМИЯ НАДПОЧЕЧНИКОВ
Область надпочечников необходимо исследовать тонкими срезами (толщиной 3 мм или 5 мм). На серии компьютерных томограмм получают изображение надпочечников в аксиальной плоскости сканирования.
Правый надпочечник. Расположен на 10—20 мм кпереди от верхнего полюса правой почки. Локализуется кзади от нижней полой вены. С латеральной стороны железа отграничена от висцеральной поверхности правой доли печени ретроперитонеальной жировой клетчаткой, которая в зависимости от особенностей конституции пациента имеет различный объем. Медиальная поверхность надпочечника параллельна правой ножке диафрагмы. Нижние отделы железы расположены выше сосудистой ножки почки. Правый надпочечник локализуется примерно на 10 мм кнаружи от тела позвонка и на 5—10 мм кзади от переднего края тела позвонка (рис. 12.4).
Левый надпочечник. Медиальные отделы железы определяются кнаружи от левой ножки диафрагмы, но, в отличие от правого надпочечника, не параллельны ей. Левый надпочечник расположен кпереди от наружного края тела позвонка и верхнего полюса левой почки. Аорта локализуется медиальнее железы. Нижние отделы левого надпочечника не доходят до сосудистой ножки почки. Хвост поджелудочной железы расположен кпереди и (или) немного латеральнее левого надпочечника и у 95% пациентов визуализируется вместе с ним, поэтому он является хорошим ориентиром при поиске надпочечника. Сосуды селезенки расположены кзади от латеральных отделов железы. В ряде случаев надпочечник может соприкасаться с телом желудка (рис. 12.5).
В 51 % случаев правый надпочечник расположен выше левого, в 34% случаев правый и левый надпочечники находятся на одном уровне, в 15% наблюдений железа с левой стороны локализуется краниальнее правой.
В надпочечниках выделяют тело, латеральную и медиальную ножки.
Форма желез вариабельна. Правый надпочечник чаще имеет линейную форму, параллелен правой ножке диафрагмы. Латеральная ножка его обычно короче медиальной. Правый надпочечник может представлять собой горизонтальную линейную структуру или иметь К-образную конфигурацию. Левый надпочечник чаще имеет инвертированную V- и Y-образную форму. Встречаются линейная, треугольная и серповидная конфигурация железы. Если ножки левого надпочечника неодинаковы по длине, то превалирует размер латеральной ножки. Форма надпочечника при КТ во многом зависит от уровня сканирования. Контуры нормальной железы четкие, ровные.
Размеры надпочечников принято измерять по методике, разработанной J.Montagne и со-авт. Определяются высота, ширина и толщина железы. Высота надпочечника исчисляется суммой срезов, на которых он получил отображение. Ширина надпочечника совпадает с наибольшим вентродорсальным размером железы (расстоянием между ее передними и задними отделами).
Рис. 12.4. КТ брюшной полости на уровне надпочечников.
1 – печень; 2 — правый надпоченик; 3 — аорта; 4 селезенка.
Рис. 12.5. КТ брюшной полости на уровне надпочечников.
1 — левый надпочечник; 2 — селезенка; 3 — тело поджелудочной железы; 4 — аорта.
За толщину органа принят наибольший размер при измерении, перпендикулярном длинной оси железы или одной из ее ножек. Толщина обычно измеряется в проекции тела надпочечника, в месте соединения его латеральной и медиальной ножек.
Высота надпочечника в 92% случаев справа и в 96% наблюдений слева колеблется в пределах от 20 до 35 мм. Ширина надпочечника варьируется от 20—25 мм, однако в ряде случаев нормальный надпочечник может иметь ширину до 30 мм. Толщина органа не должна превышать 10 мм.
Плотность надпочечников составляет 15—30 HU. После введения контрастирующего вещества денситометрические показатели увеличиваются на 10—15 HU.
МРТ АНАТОМИЯ НАДПОЧЕЧНИКОВ
Локализация, размеры и форма надпочечников в МРТ-изображении не отличаются от указанных параметров при КТ. Исследование в корональной плоскости позволяет более четко оценить месторасположение железы, ее высоту (рис. 12.6).
МРТ позволяет визуализировать правый надпочечник у 99% взрослых пациентов, левый надпочечник — у 91 % обследуемых.
Нормальные надпочечники на Т1- и Т2-ВИ представляют собой однородные, гипоинтен-сивные структуры, которые хорошо дифференцируются на фоне окружающей жировой клетчатки (рис. 12.7). При использовании Т2-В И сигнал от паренхимы надпочечников сравним с таковым от паравертебральных мышц; незначительно превышает сигнал от печени и коркового вещества почек и значительно превосходит сигнал от ножек диафрагмы (рис. 12.8).
Применение STIR ИП дает возможность подавить сигнал от ретроперитонеальной жировой клетчатки и хорошо визуализировать надпочечники, которые имеют умеренно гиперинтенсивный сигнал. Ни одна из импульсных последовательностей не позволяет различить корковое и мозговое вещество железы. После введения контрастирующего препарата его накопление наступает через 2—5 минут. Надпочечники представляют собой яркие гиперинтенсивные структуры. «Вымывание» контрастирующего вещества происходит быстро — в течение 5 минут.
Характерные КТ- и МРТ-признаки имеют надпочечники новорожденного (в первые две недели постнатального развития). Их отличают большие размеры, обусловленные значительным объемом зародышевой фетальной зоны. Клетки фетальной зоны бедны липидами, поэтому на Т2-ВИ и STIR ИП сигнал от надпочеников превышает данный показатель у взрослого человека.
Рис. 12.6. МРТ надпочечников. Т1-ВИ, корональная плоскость.
1 — правый надпочечник; 2 — левый надпочечник; 3 — правая почка; 4 — левая почка.
Рис. 12.7. МРТ надпочечников. Т1-ВИ, аксиальная плоскость.
1 —левый надпочечник; 2 — правый надпочечник.
Рис. 12.8. МРТ надпочечников. Т2-ВИ, аксиальная плоскость.
1 — левый надпочечник; 2 — правый надпочечник.
Пучковая зона
Эта зона ответственна за синтез глюкокортикостероидов. Они отвечают за белковый, углеводный и жировой обмены в организме. Тесно взаимосвязаны с выработкой инсулина и катехоламинов.
Глюкокортикостероиды снижают иммунный ответ, угнетают воспалительные процессы, постепенно подавляя их.
Один из гормонов пучковой зоны – кортизол. Он принимает участие в углеводном обмене, сохраняет энергетические ресурсы организма. Уровень кортизола в организме постоянно меняется – в утренние часы его больше, чем в вечерние или ночью.
Клубочковая зона
Клубочковая зона коры надпочечников отвечает за минеральный обмен в организме. Продуцируемые здесь гормоны нормализуют функционирование почечных канальцев, поэтому из организма выходит избыточная жидкость, что, в свою очередь, держит в норме показатели артериального давления.
В клубочковой зоне происходит секреция таких гормонов:
- Альдостерон. Его функция – в поддержании баланса ионов натрия и калия в крови. Гормон принимает участие в водно-солевом обмене, улучшает циркуляцию крови, увеличивает кровяное давление.
- Кортикостерон – гормон с малой активностью, участвует в минеральном балансе.
- Дезоксикортикостерон – тоже регулирует водно-солевой баланс, придает силу скелету и мышечной ткани.
Наши клиники в Санкт-Петербурге
Медицентр на Пионерской Аллея Поликарпова 6к2 Приморский район
- Пионерская
- Удельная
- Комендантский
Медицентр Юго-Запад Пр.Маршала Жукова 28к2 Кировский район
- Автово
- Проспект Ветеранов
- Ленинский проспект
Медицентр в Девяткино Охтинская аллея 18 Всеволожский район
- Девяткино
- Гражданский проспект
- Академическая
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
Записаться на прием
Надпочечники состоят из внутреннего мозгового слоя и коры. В верхней части коры, представляющей собой клубочковую зону, вырабатывается альдостерон. Внутренний слой производит синтез половых гормонов. В мозговом слое вырабатывается норадреналин и адреналин. Основным глюкокортикоидом является кортизол. Они занимаются регуляцией обмена веществ, оказывают противовоспалительное действие. Альдостерон является наиболее активным минералокортикоидом. Он увеличивает вывода калия и снижает выведение натрия из организма.
Функции надпочечников в организме:
- защитно-приспособительная;
- контроль обменных процессов;
- выработка гормонов, в том числе и половых.
Как проявляются заболевания надпочечников?
При нарушении баланса гормонов в организме происходит сбой в его работе. Симптомы появляются по схеме зависимости, то есть конкретное продуцируемое в надпочечниках вещество отвечает за присущий только ему симптом. Например, при дефиците альдостерона из организма вместе с мочой выводится натрий, что понижает показатели давления, значительно увеличивает содержание калия в крови.
Чтобы избежать тяжелых последствий, необходимо обратиться к врачу при первых признаках заболеваний надпочечников. К ним относятся:
- слабость в мышцах;
- постоянную усталость;
- сильное похудение следствие снижения аппетита;
- низкую стрессоустойчивость;
- высокую раздражительность;
- быструю и постоянную утомляемость;
- проблемы со сном;
- головокружение, головные боли.
Далее – наиболее распространенные заболевания надпочечников, которые имеют свои симптомы и причины, требуют определенной тактики лечения.
Гиперфункция мозгового слоя надпочечников
113114115116117118119>
Функция мозгового слоя усиливается, как правило, при попадании организма в экстремальные условия, действии ноцицептивных (от лат. посеге
— вредить) раздражителей. В этих условиях происходит активация симпатоадреналовой системы, что является частью общего адаптивного синдрома. Иногда в основе гиперфункции лежит образование опухоли из клеток мозгового слоя надпочечника или вненадпочечниковой хромафинной ткани — хромаффиномы. Она чаще бывает доброкачественной (феохромоцитома) и реже злокачественной (феохромобластома). Опухоль встречается относительно редко — по данным вскрытий, в 0,04%. Однако среди больных артериальной гипертензией она встречается намного чаще. Размеры опухоли колеблются в широких пределах — от микроскопических до опухолей массой 3,5 кг. Клетки хромаффиномы секретируют катехоламины — адреналин, норадреналин, предшественник — дофамин и иногда серотонин. Количество и соотношение секретируемых продуктов резко варьируют, что создает большие различия в клинических проявлениях заболевания.
Сердечно-сосудистый синдромпроявляется прежде всего пароксизмальным или постоянным повышением артериального давления. Наблюдаются различные изменения деятельности сердца: тахикардия или брадикардия, нарушения ритма типа экстрасистолии, блокады пучка Гиса, мерцания предсердий.
Нарушение обмена веществхарактеризуется симптомами умеренного диабета, тиреотоксикоза, гиперхолестеринемии. Для больных с феохромоцитомой типично раннее развитие атеросклероза.
Нервно-психический синдромпроявляется во время пароксизмов головокружением, головной болью, галлюцинациями, повышенной возбудимостью нервной системы, судорогами.
Реже феохромоцитома сопровождается желудочно-кишечным синдромом.Он выражается в тошноте, рвоте, запорах, иногда в изъязвлении стенки желудка кишечника с последующим развитием кровотечения.
Напротив, гипофункция мозгового слоя надпочечников может служить одним из патогенетических факторов гипотонических состояний.
Патофизиология щитовидной железы
Гипертиреоз
Гипертиреоз— синдром, вызываемый повышением функции щитовидной железы.Резко выраженный гипертиреоз называют тиреотоксикозом. Гипертиреоз, в зависимости от места, где произошло первичное нарушение, можно разделить на первичный, вторичный и третичный. Причинами первичного гипертиреозаможет быть нарушение функции щитовидной железы, развивающееся при таких болезнях, как диффузный токсический зоб (базедова болезнь, болезнь Грейвса, болезнь Парри), тиреотоксическая аденома щитовидной железы. Причиной вторичного гипертиреозаможет являться развитие ТТГ-секретирующей опухоли аденогипофиза, а причиной третичного гипертиреоза— нарушение в гипоталамусе.
В целом наиболее частой причиной развития гипертиреоза является диффузный токсический зоб. Считается, что при этом заболевании в организме вырабатываются тиреоидстимулирующие антитела, которые, подобно ТТГ, способны связываться с рецепторами на базальной мембране тиреоцита, что приводит к активации клетки. Одновременно уровень ТТГ в крови больных снижен по механизму обратной связи.
Гипертиреоз сопровождается нарушением энергетического и повышением основного обмена, усилением потребления кислорода, расстройством различных видов обмена, похуданием, нарушением функции ЦНС, сердечно-сосудистой системы и других органов.
Энергетический обмен.Трийодтиронин разобщает окисление и фосфорилирование в митохондриях клеток, в результате чего энергия окисления НАД2Н и НАДФ2Н не аккумулируется в АТФ и рассеивается. Уменьшение синтеза АТФ увеличивает концентрацию его предшественников — АДФ и неорганического фосфата, также изменяется перенос АДФ в митохондрии, поскольку трийодтиронин связывается с переносчиком АДФ транслоказой, что, в свою очередь, усиливает окислительные процессы и тем самым рассеивание энергии. Это ведет к увеличению основного обмена.
Углеводный обмен.При гипертиреозе усиливается обмен углеводов, увеличивается утилизация глюкозы тканями. Активируется фосфорилаза печени и мышц, следствием чего является усиление гликогенолиза и обеднение этих тканей гликогеном. Повышается активность гексокиназы и всасывание глюкозы в кишечнике, что сопровождается алиментарной гипергликемией. Активируется ин-
сулиназа печени. Это в совокупности с гипергликемией вызывает напряженное функционирование инсулярного аппарата и в случае его неполноценности может привести к развитию сахарного диабета. Кроме того, усиление пентозофосфатного пути обмена углеводов способствует повышенному образованию НАДФ2Н.
Белковый обмен.На белковый обмен тиреоидные гормоны в больших дозах оказывают главным образом катаболическое действие, что приводит к отрицательному азотистому балансу. Усиливается выделение азота, фосфора и калия с мочой, указывающее на клеточный распад. Увеличивается выделение аммиака. В крови повышается уровень остаточного азота и азота аминокислот. С повышенным катаболизмом белка связано развитие таких симптомов диффузного токсического зоба, как атрофия мышц и остеопороз.
Жировой обмен.В связи с усилением энергетического обмена больные тиреотоксикозом худеют главным образом за счет уменьшения запасов жира в жировых депо. Уменьшение запасов жиров происходит вследствие: а) мобилизации жиров из депо за счет сенсибилизации симпатических нервных окончаний в жировой ткани; б) ускорения окисления жиров в печени; в) торможения перехода углеводов в жиры. В связи с усилением окисления жира увеличивается образование кетоновых тел. При одновременном дефиците углеводов это приводит к нарушению их окисления и, следовательно, к гиперкетонемии и кетонурии. Повышенный распад жиров приводит к развитию общего похудания больных диффузным токсическим зобом.
Водный и минеральный обмен.Повышение в крови концентрации тиреоидных гормонов вызывает увеличение: а) относительного содержания воды в организме в связи с похуданием; б) объема плазмы; в) скорости фильтрации воды через капиллярные стенки; г) диуреза в связи с усилением почечного кровотока и клубочковой фильтрации; д) потоотделения; е) потери воды с выдыхаемым воздухом. При этом усиливается выведение кальция, фосфора и калия из организма.
Центральная нервная система и другие органы.Тиреоидные гормоны оказывают выраженное влияние на центральную нервную систему. Возбудимость коры головного мозга повышается. В клетках коры, ствола головного мозга и передних рогов спинного мозга развиваются токсически-дегенеративные изменения. Меняется возбудимость гипоталамических вегетативных центров, а в связи с этим и функция внутренних органов.
Со стороны сердечно-сосудистой системы отмечаются стойкая тахикардия, наклонность к мерцанию предсердий. В основе этого явления лежит повышение чувствительности миокарда к адреналину и норадреналину в связи с увеличением количества бета-адренергических рецепторов под влиянием тиреоидных гормонов. Возможно также, что при распаде тиреоидных гормонов образуются активные продукты, способные функционировать как псевдокатехоламины. Усиление работы сердца вызывает его гипертрофию и дистрофические изменения. Нарастание возбуждения симпатического отдела нервной системы приводит к повышению тонуса артериол и развитию гипертонии, развитию тремора. Снижение количества гликогена в печени уменьшает ее дезинтоксикационную функцию и способность синтезировать белки. Повышена влажность и температура кожи. Развивающийся в ряде случаев при диффузном токсическом зобе экзофтальм (пучеглазие) (рис. 20-15), так же как и изменение кожи голеней и кистей (акропатия), может быть следствием аутоиммунного повреждения тканей.
Рис. 20-15.Тиреотоксикоз у женщины 33 лет (по Н.А. Шерешевскому)
Гипотиреоз
Гипотиреоз— состояние, возникающее при недостатке тиреоидных гормонов в организме.Так
же как и гипертиреоз, он может быть первичным, вторичным и третичным. Первичный гипотиреозвстречается при тиреоидите Хасимото, дефектах биосинтеза тиреоидных гормонов, тиреоидэктомии, лечении радиоактивным йодом, недостаточном поступлении йода в организм и других патологических процессах в железе. Вторичный и третичный гипотиреозявляются следствием выпадения регуляторных влияний (поражения гипофиза, дефицит тиролиберина). Наиболее выраженную форму гипотиреоза у взрослых
называют микседемой.Синдром, который развивается у детей в связи с полной недостаточностью щитовидной железы, называют кретинизмом.Кретинизм характеризуется выраженной задержкой роста и своеобразной внешностью больного (рис. 20-16). В основе кретинизма лежит, как правило, аплазия щитовидной железы.
Тиреоидэктомия в эксперименте сопровождается отставанием в росте молодых животных, задержкой роста трубчатых костей и полового развития. Возникают отклонения от нормы во внешнем виде. Меняется конфигурация черепа — укорачивается передняя часть лица, а задняя приобретает шаровидную форму, останавливается развитие зубов. У собак конечности становятся толстыми, движения — неуклюжими, прекращается рост шерсти. Развивается слизистый отек подкожной клетчатки вследствие задержки воды, хлористого натрия и накопления в соединительной ткани мукопо-
лисахаридов, обладающих гидрофильными свойствами. При хорошем содержании животные могут жить месяцы и годы.
При гипотиреозе наблюдаются следующие нарушения обмена веществ и функций органов:
Энергетический обмен.Гипотиреоз сопровождается уменьшением интенсивности окислительных процессов, что приводит к снижению основного обмена.
Белковый обмен.При функциональной недостаточности щитовидной железы снижается интенсивность синтеза белка. Свидетельством этого является торможение скорости включения метионина в белки тканей. При этом усиливается катаболизм аминокислот, уменьшается содержание РНК в тканях.
Углеводный обмен.Интенсивность обмена углеводов падает. Повышается содержание гликогена в печени в связи со снижением активности фосфорилазы. В результате ослабления активности гексокиназы уменьшается всасывание глюкозы в кишечнике. Следствием замедления окислительных процессов в тканях может быть развитие гиперкетонемии.
Жировой обмен.Скорость синтеза холестерина в печени и надпочечниках снижается, однако еще более замедляется его распад, что ведет к гиперхолестеринемии и способствует развитию атеросклероза.
После тиреоидэктомии у собак снижается возбудимость центральной нервной системы. У людей при гипотиреозах отмечается замедление психических реакций, ослабление памяти, в тяжелых случаях — слабоумие.
Эндемический зоб.Особой формой гипотиреоза является эндемический зоб. Он развивается в определенных географических районах, в которых население не получает с пищей достаточного количества йода. Недостаток йода снижает синтез тиреоидных гормонов, что по механизму обратной связи усиливает секрецию ТТГ гипофизом. Это вызывает гиперплазию железы, что вначале компенсирует недостаток тиреоидных гормонов. Однако при продолжающемся дефиците йода эта компенсация оказывается недостаточной для образования тиреоидных гормонов, и развивается гипотиреоз, который в далеко зашедших случаях может перейти в микседему и кретинизм (рис. 20-17). Профилактическое введение йода препятствует возникновению этого заболевания. С этой целью к поваренной соли добавляют 0,002% йодистого натрия или калия. Потребление 6 г соли ежедневно означает прием 120 мкг йодида, что является оптимальной суточной дозой для взрослых.
Рис. 20-17.Группа эндемических кретинов из местечка Аарау (Германия, 1908) (по W. Falta, 1913)
113114115116117118119>
Дата добавления: 2016-07-11; просмотров: 4201; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Узнать еще:
Болезнь Аддисона
Другие названия болезни Аддисона – первичная надпочечниковая недостаточность и гипокортицизм.
Редкая патология, на которую приходится 50 – 100 случаев на один миллион в год. Диагностируют и у женщин, и у мужчин. Средний возраст – от 20 до 40 лет.
При заболевании происходит поражение всех трех зон надпочечниковой коры. Характеризуется дефицитом выработки кортикостероидов. Нарушение синтеза гормонов вызывает серьезные осложнения в организме.
Причина разрушения коры надпочечников – попавшие в организм болезнетворные микроорганизмы – вирусы, бактерии, грибки, а также иммунные нарушения.
Проявления болезни Аддисона:
- снижение показателей артериального давления;
- быстрая утомляемость, слабость, отсутствие физических сил;
- отсутствие аппетита;
- нарушение работы пищеварительной системы;
- пигментация кожных покровов, появление темных пятен на слизистых оболочках;
- озноб;
- повышение температуры тела.
Для выявления заболевания необходима сдача анализов на уровень кортизола в крови. Проводят обследование состояния коры надпочечников, функционирования желез.
Лечение – прием препаратов с содержанием кортикостероидов на протяжении всей жизни. Возможно введение гидрокортизона внутримышечно.
Болезнь Иценко-Кушинга
Относится к нейроэндокринным патологиям. Причина – сбой работы гипоталамо-гипофизарной системы в результате травмирования головного мозга или перенесенных человеком инфекций. Характеризуется продуцированием излишнего объема кортикостероидов надпочечниками.
Болезнь Иценко-Кушинга – редкая патология. Диагностируют преимущественно у женщин в возрасте от 30 до 45 лет.
Сбой в работе гипоталамо-гипофизарной системы провоцирует нарушения в организме. Утрачивается связь между надпочечниками, гипоталамусом и гипофизом. Сигналы, идущие в гипоталамус, провоцируют избыточную выработку гормонов, высвобождающих адренокортикотропный гормон (АКТГ) в гипофизе, что стимулирует выброс вещества в кровь. Излишнее количество АКТГ влияет на надпочечники, которые начинают усиленного вырабатывать много кортикостероидов.
При прогрессировании патологии происходит видимое увеличение гипофиза и надпочечников в размерах.
Признаки болезни Иценко-Кушинга:
- головные боли, мигрени;
- прогрессирующая гипертония;
- атрофия мышц;
- формирование лунообразной формы лица;
- отсутствие менструации у женщин;
- развитие остеопороза;
- рост волос на лице у женщин.
Для выявления заболевании назначают сдачу анализов крови и мочи, в которых определяется избыточное количество АКТГ и кортизола. Дополнительно проводят инструментальное обследование.
Цель терапии – восстановление нарушенного обмена веществ, нормализация работы гипоталамуса, приведение в норму синтеза кортикостероидов.
Феохромоцитома
Феохромоцитома представляет собой опухоль, развивающуюся в мозговом веществе надпочечников. В ее основе – хромаффинные тела, которые способствует синтезу большого количества катехоламинов.
Причина – артериальная гипертензия и катехоламиновые кризы.
Симптомы феохромоцитомы:
- высокое артериальное давление, гипертонические кризы;
- головная боль;
- повышенное потоотделение;
- одышка;
- обезвоживание организма;
- судороги;
- кардиомиопатия;
- высокий уровень сахара в крови.
Для диагностики заболевания назначают анализы для определенияметаболитов катехоламинов в моче и крови. Для выявления образования применяются аппаратные методы – МРТ и ультразвуковое сканирование.
Лечение медикаментозное, направлено на снижение степени выраженности пароксизмальных приступов.
Гиперальдостеронизм
Другие название патологии – синдром Кона. Состояние, при котором в коре надпочечников вырабатывается излишнее количество альдостерона и дезоксикортикостерона.
Причины гиперальдостеронизма – злокачественное образование в коре надпочечников или гиперплазия тканей коры.
Синдром Кона имеет первичную и вторичную степени развития. Симптомы первичной степени заболевания:
- повышение артериального давления;
- головные боли;
- нарушение сердечного ритма;
- кардиалгия – боли в левой части груди;
- снижение остроты зрения.
Симптомы вторичной степени возникают в результате избытка калия и дефицита натрия:
- отеки;
- хроническая почечная недостаточность;
- деформация глазного дна;
- артериальная гипертензия.
Диагностические мероприятия включают определение уровня калия и натрия, альдостерона в крови и моче.
Терапия зависит от результатов проведенного обследования. Чаще это медикаментозное лечение с назначением гормональных препаратов. При наличии опухоли возможно проведение операции.
Симптомы заболеваний надпочечников
Проявления болезней надпочечников зависят от того, какой именно гормон или гормоны вырабатывается в недостаточном или избыточном количестве. Например, избыток минералокортикоидов обусловливает повышение артериального давления и снижение уровня калия, избыток половых гормонов вызывает нарушение полового развития, чрезмерный рост волос на лице и т.д. Угрожающим жизни состоянием является острая надпочечниковая недостаточность, возникающая при резком снижении или прекращении выработки гормонов корой надпочечников.
Гиперплазия коры надпочечников
Это увеличение в размере коры надпочечников, что ведет к усиленному синтезу андрогенов. Основная причина – генетическая, то есть заболевание является врожденным.
Выделяют три основные формы гиперплазии:
- Простая вирилизирующая. Происходит усиление синтеза андрогенов, в результате увеличиваются половые органы, мышечная ткань, ускоренно растут волосы на всем теле независимо от пола больного человека.
- С синдромом утраты соли. Характеризуется избытком калия и дефицитом других гормонов.
- Гипертоническая. Происходит избыточное продуцирование андрогенов и кортикостероидов, в результате развивается артериальная гипертензия, ухудшается зрительная функция.
Симптомы гиперплазии коры надпочечников:
- ранний рост волос на теле и на половых органах;
- рост меньше нормы;
- грубый голос;
- проблемы с памятью;
- частые психозы;
- слабость мышечной системы.
Признаки появляются в детском возрасте. Для уточнения диагноза назначают сдачу анализов, лабораторные исследования.
Лечение медикаментозное, включает постоянный прием гормональных препаратов. При тяжелом течении заболевания показано хирургическое вмешательство.
Гиперфункциональные состояния коры надпочечников
Повышенная секреция мужских половых гормонов (андрогенов) у женщин приводит к состоянию, которое называется «гиперандрогения» (симптомами заболевания являются избыточное оволосение тела, невынашивание беременности, нарушение менструального цикла, отсутствие овуляции, бесплодие, ожирение, огрубение голоса, угревидная сыпь на коже).
Избыток мужских гормонов у женщин оказывает влияние на ее способность зачать и вынашивать детей. Беременная женщина с гиперандрогенией должна быть под строгим контролем участкового врача женской консультации в связи с возможной угрозой прерывания беременности. Необходимо проводить периодический контроль уровня мужских половых гормонов в ее организме, для того чтобы корректировать назначенную схему лечения.
Как правило, гиперандрогения лечится с помощью синтетических аналогов кортизола (преднизон, дексаметазон). Эти препараты назначаются с целью подавить влияние гипофиза на надпочечники.
Возникновение адреногенитального синдрома связано с дефицитом С21-гидроксилазы. В настоящее время во врачебной практике чаще используется термин «дисфункция» или «гиперфункция надпочечников».
| Адреногенитальный синдром (гиперандрогения) | |
| Форма дисфункции надпочечников | Проявления |
| Классическая форма | При классической форме адреногенитального синдрома повышенная секреция андрогенов начинается еще внутриутробно, на 9-10 неделе после гестации. Избыток мужских половых гормонов нарушает формирование наружных половых органов у будущей девочки (внутренние половые органы плода женского пола к 9-10 неделе внутриутробного развития уже имеют присущее женскому полу строение). Вторым проявлением врожденной гиперандрогении является гиперплазия надпочечников. Такой ребенок после рождения должен быть поставлен на учет у детского эндокринолога. |
| Пубертатная форма врожденной дисфункции надпочечников | Адреногенитальный синдром начинает проявляться у ребенка в период полового созревания, когда гормональная функция коры надпочечников начинает усиливаться. Как правило, заболевание начинает проявляться у девочек в 12-13 лет. Характерные проявления пубертатной формы адреногенитального синдрома:
|
| Постпубертатная форма | Обычно обнаруживается в 25-29 лет, как правило, в связи с неудачной беременностью (выкидыш, медицинский аборт, неразвивающаяся беременность). Больные жалуются на нарушения в менструальном цикле — на тенденцию к задержкам менструаций и на общее удлинение цикла. В связи с поздним развитием гиперандрогении ее проявления имеют стертый характер: избыточное оволосение выражено скудно, молочные железы имеют нормальное развитие, фигура молодой женщины развита по женскому типу. |
При секреции повышенных доз гормонов надпочечников возникают определенные клинические проявления. Избыточное выделение кортизола приводит обыкновенно к синдрому Кушинга, а «лишняя» продукция мужских половых гормонов у женщин — к маскулинизации. В норме кортизол тормозит продукцию адренокортикотропина (АКТГ), выделяемого гипофизом. Хроническая недостаточность кортизола проявляется адреногенитальным синдромом (в крови резко возрастает число мужских половых гормонов).
Недостаточность коры надпочечников
Это нарушение функционирования надпочечников аутоиммунной природы. Бывает двух видов – острая и хроническая.
Хроническая недостаточность коры надпочечников возникает в результате деструктивных изменений в железистых тканях органа. Основные причины – перенесенные инфекционные заболевания, опухоль гипофиза или макроаденома, омертвление или угнетение передней доли гипофиза.
Острая форма развивается на фоне хронической. Самостоятельно почти не возникает, исключение – сепсис или внезапное кровоизлияние в надпочечниках.
Симптомы надпочечниковой недостаточности:
- слабость, постоянный упадок сил;
- снижение аппетита, в результате этого – резкое снижение массы тела;
- гиперпигментация кожных покровов;
- артериальная гипотензия;
- снижение уровня сахар в крови;
- частое мочеиспускание;
- тошнота, переходящая в рвоту;
- нехарактерный стул.
Дисфункции надпочечников
Гипоадрения
Стресс
— это напряжение организма, связанное с неблагоприятным на него воздействием или появлением угрожающей жизни или благополучию индивида ситуации. Проще говоря, стресс является защитной реакцией от опасных воздействий. Стрессор (фактор, вызывающий стресс) может быть как физиологическим, так и психологическим. Организм человека реагирует на стресс так, как заложено в нем с древних времен — мобилизуя свои силы и переходя в режим полной боевой готовности. В качестве ответа на опасность наши надпочечники начинают вырабатывать повышенное количество гормонов.
Итак, как же наш организм отвечает на стресс и адаптируется к нему?
Стресс активизирует мощный выброс в кровь кортизола и адреналина. В результате этого, повышается артериальное давление, учащается ритм сердца, а тонус мышц повышается. В кратковременном напряжении всех ресурсов организма нет ничего страшного, гораздо хуже, если стресс «входит в привычку» и становится хроническим. Постоянная нервная перегрузка приводит к истощению функции надпочечников — гипоадрении.
Второй причиной гипоадрении может быть беременность
.
Большой нагрузкой на надпочечники, как матери, так и растущего плода является беременность. Обычно надпочечники плода начинают работать только к шестому месяцу беременности (началу третьего триместра). Если беременная находится в состоянии гипоадрении (недостаточности функции надпочечников), то надпочечники плода начинают работать «за двоих», поддерживая ее.
Поэтому многие женщины в финальном триместре чувствуют прилив сил, по сравнению с предшествующими неделями беременности. Тем не менее, стресс, которые испытывают надпочечники, может оказать прямое влияние на здоровье родившегося ребенка: он может выказывать признаки гипоадрении. В последующем это отражается на состоянии здоровья младенца:
- снижаются возможности иммунной системы (часто болеющий ребенок)
- аллергическая настроенность организма
Мать же, оказавшись без поддержки надпочечников плода, после рождения ребенка возвращается в состояние гипоадрении, в результате чего приходится лечить обоих — и маму, и ребенка.
Тиричные патологии надпочечников подразделяются на гиперфункциональные
и
гипофункциональные
.
Воспаление надпочечников
Воспалительные процессы в надпочечниках возникают чаще всего на фоне туберкулезного поражения их коры. Особенность патологии – в медленном развитии.
Характерные симптомы воспаления:
- ощущение постоянной усталости;
- низкая стрессоустойчивость;
- регулярные ноющие головные боли;
- неприятный запах изо рта;
- тошнота, переходящая в рвоту.
При запущенной форме высока вероятность развития хронического воспалительного процесса.
Туберкулез надпочечников
Туберкулез надпочечников – редкая патология. Для нее характерно накапливание кальцинатов в тканях надпочечников.
Чаще диагностируют в детском и подростковом возрасте. Причина – проникновение туберкулезной палочки из зараженных легких в надпочечники через общий кровоток.
Симптомы туберкулеза надпочечников:
- низкое артериальное давление;
- нарушение работы желудочно-кишечного тракта, выражающееся диарей, тошнотой с рвотными приступами;
- гипогликемия;
- постоянная слабость, ощущение усталости;
- дистрофия миокарда.
Киста
Это доброкачественное образование в тканях надпочечников. Опухоль появляется редко и становится опасной только при перерождении в злокачественную. Опасно состояние, при котором происходит разрыв кисты надпочечника.
Симптомы опухоли:
- боли в пояснице, спине, по бокам;
- нарушение функционирования почек;
- увеличение надпочечников в размере;
- повышение артериального давления в результате сдавливания почечной артерии.
Диагностика кисты надпочечников затруднена из-за ее небольших размеров. Выявить патологию можно только при прогрессировании и росте опухоли.
Опасные опухоли
Если киста является доброкачественным образованием, то есть ряд опухолей, склонных к озлокачествлению.
Наиболее частые из них:
- альдостерома;
- андостерома;
- глюкокортикостерома;
- кортикоэстрома.
Точные причины развития образований установить сложно, но высока вероятность их гормональной активности на фоне следующих провоцирующих факторов:
- гиперплазия клеток и разрастание тканей надпочечников;
- избыточное количество продуцируемых гормонов;
- онкологические заболевания щитовидной железы;
- заболевания, связанные с врожденными патологиями кожи, глазной оболочки, сосудов головного мозга.
Локализация опухолей различна. Они могут формироваться и в мозговом, и в корковом слоях. Характерные симптомы:
- высокие показатели артериального давления;
- опоздание процесса полового развития;
- частая тошнота, переходящая в рвоту;
- боли в животе, в области груди;
- изменение цвета кожи на лице – бледнеет, краснеет, приобретает синюшный оттенок;
- резкое изменение уровня глюкозы в крови;
- сухость во рту;
- судороги;
- тремор конечностей;
- повышенная раздражительность, возбудимость;
- повышенная тревожность, постоянное чувство страха.
Гипофункциональные состояния коры надпочечников
Хроническая недостаточность надпочечников называется болезнью Аддисона. Это заболевание характеризуется тем, что надпочечники теряют способность производить гормоны в достаточной мере (особенно кортизол).
Основные симптомы болезни Аддисона:
- Слабость, усталость в течение длительного времени
- Потеря мышечной массы
- Снижение аппетита
- Тошнота, рвота, диарея, нарушение глотания, тянущие боли в животе
- Гипотония (сниженное артериальное давление)
- Появление пятен и гиперпигментации на коже
- Депрессия, вспыльчивость, агрессивность, раздражительность, внутреннее напряжение, нервозность, тревожность, плаксивость
- Изменение вкусовых предпочтений, пристрастие к соленому
- Понижение уровня глюкозы в крови
- Исчезновение менструаций у женщин
- Изменения в составе крови (повышенное количество эозинофилов)
- Судороги, парестезии, тремор рук и головы
- Повышенное выделение мочи
- Обезвоживание (дегидратация) организма
- Нарушения в работе сердца (тахикардия)
Острым состоянием, которое может угрожать жизни пациента является «аддисонический криз». Заболевание лечится синтетическими кортикостероидами (доза препарата устанавливается после осмотра пациента).