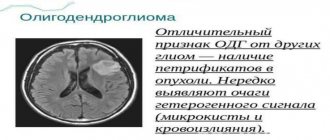
Причины гипоксии головного мозга
Примерно 20% от всего объема циркулирующей в организме крови поступает в головной мозг. Вместе с клетками крови к органу доставляется кислород и иные полезные вещества, которые необходимы для поддержания его работоспособности.
Различают эндогенную и экзогенную типы гипоксии. Причиной развития экзогенного кислородного голодания головного мозга становится снижение концентрации кислорода в окружающей среде, а именно, во вдыхаемом воздухе. Часто подобная ситуация наблюдается при подъеме в горы, поэтому такое состояние организма называют Высотной или Горной болезнью. Привести к экзогенному кислородному голоданию также способно резкое падение барометрического давления. При этом говорят о развитии у человека декомпрессионной болезни.
На эндогенное кислородное голодание указывают в том случае, когда уровень кислорода в воздухе понижен, а барометрическое давление остается в норме. Такая ситуация может случиться при нахождении человека в шахтах, а колодцах, в подводной лодке, либо во время операции при погрешностях в работе аппарата, отвечающего за подачу кислорода пациенту, находящемуся под наркозом.
Также гипоксия головного мозга может развиваться при патологических состояниях организма. В связи с этим, различают:
- Гипоксия головного мозга, которая развивается на фоне нарушений в органах дыхательной системы.
Приводить к дыхательной гипоксии головного мозга способны следующие причины:
- Альвеолярная гиповентиляция. Это может наблюдаться при нарушении проходимости дыхательных путей, например, на фоне воспалительного процесса в легких, при попадании в дыхательные пути инородного тела, по причине спазма дыхательных путей. Также к гипоксии головного мозга способны приводить: пневмония, отек легкого, пневмоторакс, скопление экссудата в плевральной полости. Причиной умеренной гипоксии головного мозга нередко становятся нарушения в подвижности грудной клетки, паралич дыхательной мускулатуры, а также ее спазм на фоне столбняка или миастении. Альвеолярная гиповентиляция может приводить к кислородному голоданию головного мозга при нарушении процессов регуляции дыхания, когда на дыхательный центр воздействуют патогенные факторы. К иным причинам относят: кровоизлияния в органы дыхания, наличие в них опухоли, травмирование продолговатого мозга, передозировка наркотическими или снотворными препаратами, сильные боли, которые возникают у человека во время выполнения дыхательных движений.
- Сбой вентиляционно-перфузионных связей развивается по причине нарушения проходимости дыхательных путей на фоне бронхоспазма, эмфиземы легких, пневмосклероза.
- Чрезмерное шунтирование венозной крови, что наблюдается при врожденных аномалиях развития сердца.
- Затрудненная диффузия кислорода. Причиной становится эмфизема легкого, асбестоз, саркоидоз легкого, интерстициальный отек легкого.
- Гипоксия, которая развивается на фоне тех или иных нарушений кровообращения, приводящих к недостаточному кровоснабжению тканей головного мозга. Причинами являются: массивная потеря крови, обезвоживание организма при ожогах или холере и пр. Сюда же относят нарушения в работе сердечной мышцы, например, инфаркт миокарда или кардиосклероз, тампонаду сердца, перегрузки сердца. Зачастую факторы могут встречаться в различных комбинациях. Циркуляторная гипоксия головного мозга развивается на фоне тяжелых инфекционных заболеваний, выраженных аллергических реакций, нарушениях электролитного баланса, при приеме глюкокортикоидов, при повышении вязкости крови, при острой и хронической сердечной недостаточности, при коллапсе и пр.
- Сниженная кислородная емкость крови, приводящая к развитию гипоксии головного мозга, может стать следствием таких факторов, как: выраженная анемия с резким падением уровня гемоглобина в эритроцитах. Это часто наблюдается при таких заболеваниях, как туберкулез, язвенная болезнь желудка и кишечника, при отравлении гемолитическими ядами, при массивных ожогах, при малярии, при воздействии на организм ионизирующей радиации, на фоне нехватки витаминов и железа из пищи.
- Тканевая гипоксия головного мозга развивается в том случае, когда ткани организма утрачивают способность поглощать кислород из крови. Подобная ситуация развивается на фоне отравления цианидами, при передозировке барбитуратами, антибиотиками, при воздействии на организм отравляющих веществ различного происхождения. Также спровоцировать тканевую гипоксию головного мозга способен дефицит тиамина, рибофлавина и иных витаминов.
- Гипоксия головного мозга по смешанному типу развивается тогда, когда к ней приводят несколько факторов одновременно. Стоит отметить, что любая тяжелая гипоксия протекает по смешанному типу, например, при различных видах травматического шока или во время комы.
Введение
В организме человека существует специальная система защиты мозга от проникновения в него крупных молекул, в том числе инфекционных агентов — это гематоэнцефалический барьер (ГЭБ). Давайте подробнее рассмотрим его структуру (рис. 1). Первая линия защиты — плотный стой эндотелия капилляров, соединенных плотными контактами. В отличие от большинства капилляров тела, в них нет крупных щелей (пор) для прохождения некоторых белков плазмы [1]. Далее на пути к мозгу находятся перициты (клетки соединительной ткани) и астроциты (вспомогательные клетки в нервной ткани), которые механически не позволяют пройти молекулам крупнее определенного размера. Гематоэнцефалический барьер не пропускает вещества более 400–500 Да по массе, в зависимости от свойства вещества. (Для сравнения, сывороточный альбумин человека, самый распространенный белок в крови, имеет массу 65 000 Да). Также барьер непроницаем для ионов, но пропускает жирорастворимые вещества, воду, кислород, углекислый газ, некоторые обезболивающие и алкоголь (рис. 1).
Рисунок 1. Схема строения гематоэнцефалического барьера.
Э — клетки капилляров, соединенные плотными контактами; A — вещества, не проникающие через ГЭБ; B — вещества, проникающие через ГЭБ каким-либо способом, описанным ниже. Стрелками обозначены белковые системы транспорта веществ внутрь клетки и из нее.
рисунок автора статьи
Таким образом, долгое время считалось, что мозг полностью защищен от проникновения некоторых веществ из крови, пока не было обнаружено возможности прохода через ГЭБ. Такой способ доставки нужен прежде всего для доставки лекарств в нервную систему, поэтому было важно найти способы преодолеть барьер: ослабить клеточные контакты эндотелия (клеточного слоя) капилляров мозга, использовать системы транспорта веществ через мембрану капилляров или проникнуть в мозг с помощью эндоцитоза [2]. У данных способов есть свои недостатки, например, разрушение плотных контактов эндотелия приводило к местному накоплению веществ в мозге, повышению внутричерепного давления и требовало значительного времени на восстановление барьера [3]. Использование систем транспорта растворимых в воде метаболитов для доставки действующего вещества в мозг накладывает ограничения на само вещество. В данном случае оно должно либо имитировать «привычный» для данного белка-транспортера метаболит клетки, либо связываться с метаболитом для прохождения через мембрану [4]. Транспорт веществ путем эндоцитоза (захвата внешнего материала) клетками эндотелия тоже имеет свои недостатки — неспецифический эндоцитоз сведен к минимуму в капиллярах мозга, а специфический эндоцитоз часто включает в себя частичное пропускание вещества. Например, при доставке ионов железа посредством белка ферритином этот белок связывается с рецептором на эндотелии капилляра, проникает в клетку, высвобождает ионы железа для их дальнейшего транспорта в мозг, а потом удаляется из клетки обратно в просвет капилляра [5]. У всех перечисленных выше способов есть общий нюанс — вещество попадает в мозг через кровь, а значит, вещество распределяется равномерно по всему организму, поэтому нужно учитывать его системный эффект. Это накладывает дополнительные ограничения и увеличивает время испытания нового лекарства. В последние десятилетия ученые пытались преодолеть барьер и доставить лекарства с помощью наночастиц, введенных в кровь [6–8].
Наночастицы — собирательное название для группы веществ размером от 1 до 1000 нм. Они могут иметь различаться по форме и своим свойствам, в зависимости от пути преодоления ГЭБа. Это могут быть различные полимеры, натуральные или синтетические, или металлические частицы. Однако пока что наночастицы показывают не лучшие результаты в качестве транспортеров лекарств через барьер, если их вводить в кровь, а способ их проникновения через барьер — все еще спорный вопрос [9]. Как отметил Франческо Элдро, было потрачено много времени на изменение (модификацию) действующих веществ в составе лекарств для преодоления барьера, но гораздо меньше изучали способы их проникновения в мозг [10], [11].
Существуют способы проникнуть в нервную систему, даже минуя стадию попадания в кровь. Конечно, можно просверлить отверстие в черепе и ввести вещество иглой через барьер — это довольно эффективный способ преодолеть ГЭБ. Единственный недостаток в том, что введенное вещество практически не распространяется по мозгу [12]. Но есть и гораздо менее инвазивный вариант — проникнуть в мозг через носовую полость в обход ГЭБа. Рассмотрим, почему этот способ вызывает особый интерес у ученых. Вспомним строение обонятельной системы позвоночных на примере мыши (рис. 2). В носовой полости есть специальный участок скопления рецепторных окончаний нейронов — обонятельный эпителий. От дендритов сигнал проходит через тело, транспортируется по аксону и передается митральной клетке, входящей в состав обонятельной луковицы; место передачи называется синапсом.
Рисунок 2. Строение обонятельной системы.
(a) — строение обонятельной системы мыши в разрезе. ОЭ — обонятельный эпителий, ОЛ — обонятельная луковица, ЛОТ — латеральный обонятельный тракт. (б) — cтроение обонятельной луковицы мыши. АК) — аксоны обонятельных рецепторов, ГС — гломерулярный слой, МС — митральный слой, 1 и 2 — внешний и внутренний плексиформные слои обонятельной луковицы.
рисунок автора статьи
Тела митральных клеток образуют митральный слой, а аксоны этих клеток формируют латеральный обонятельный тракт. По нему передается информация о запахах в центры головного мозга, которые обрабатывают сигнал. Из-за «доступности» такого способа попадания в мозг, который вдобавок не требует серьезных ограничений по структуре и размерам веществ, данная тема требует более подробного анализа.
Данная работа посвящена изучению процесса проникновения наночастиц в головной мозг через носовую полость. Этот путь актуален не только с точки зрения доставки лекарственных препаратов, но и с точки зрения изучения процесса проникновения вирусов в головной мозг. У всех сейчас на слуху специфический симптом коронавирусной инфекции — потеря обоняния, что свидетельствует о возможности неспецифического проникновения любого вещества в нашу нервную систему.
Особенности течения гипоксии головного мозга и приспособительные реакции организма
Степень выраженности гипоксии в различных органах и тканях может различаться. Так, при возникновении угрожающей ситуации, организм самостоятельно перераспределят кровь таким образом, что головной мозг снабжается ею лучше, чем иные органы и ткани. Этот процесс называется централизацией кровообращения. Он может включаться, например, при острой кровопотери.
Результатом такого механизма становится то, что головной мозг страдает от гипоксии меньше, чем периферические органы, например, печень или почки, где необратимые изменения развиваются не с такой высокой скоростью.
Очищаем сосуды головного мозга и всего организма
Перед тем, как приступать к работе над улучшением кровообращения, необходимо полностью очистить организм и мозг от загрязнений, укрепить сосуды. Для этого необходимо натощак пить настой лекарственных трав. Лучше всего подойдут: ромашка, тысячелистник, зверобой, липовый цвет, листья земляники, также добавлять в чай калину или рябину. Также утром натощак выпивайте стакан чистой воды с лимонным соком. Также чистку можно делать при помощи мелиссы. Залить листья кипятком и дать настояться 5 часов, затем употреблять по 50 грамм три раза в день. Чтобы мозг работал как часы, включайте в свой рацион морковь, лук, чеснок, хрен. Также полезно употреблять в пищу майский мед. Съедать по чайной ложке утром и вечером – питает мозг и укрепляет сосуды.
Как проявляется гипоксия головного мозга?
В зависимости от степени выраженности расстройств со стороны головного мозга при гипоксии, выделяют:
- Легкая степень. Это проявляется такими симптомами, как: заторможенность, оглушенность, либо, напротив, человек становится гипервозбужденным, у него наблюдается эйфория, повышается артериальное давление, учащается сердцебиение. Глазные щели становятся неравномерными по размеру в результате пареза лицевого нерва. Если не устранить патогенный фактор, оказывающий влияние на кислородное голодание головного мозга, то через несколько часов или суток, оно перейдет в следующую стадию.
- Средняя степень. У больного сохраняется парез лицевого нерва, рефлексы слизистых оболочек и сухожильные рефлексы чаще всего понижены. Время от времени возможно возникновение судорог, которые начинаются с лицевой части, а затем распространяются на туловище и конечности. Тревожность и психомоторное возбуждение повышено. Пострадавший с трудом ориентируется в пространстве, у него ухудшается память и иные когнитивные способности.
- Тяжелая степень. У больного наблюдается глубокое угнетение сознания с утратой произвольной деятельности, но рефлексы при этом сохраняется. Такое состояние называется сопорозным. Иногда уже на этой стадии человек впадает в тяжелую кому. У него развиваются судороги верхних и нижних конечностей, появляются хватательные и сосательные рефлексы, мышечный тонус падает. Возможно стойкое повышение температуры, усиление потливости и слезотечения.
- Критическая степень, которая несет угрозу жизни. Это состояние характеризуется глубокой комой, страдают все структуры головного мозга. Кожа больного холодная, мимика отсутствует, глазные яблоки находятся без движения, зрачки расширены, на свет не реагируют. Рот остается полуоткрытым, веки прикрыты, кожа цианотична. Сердце работает слабо, тонус сосудов снижен. По мере прогрессирования гипоксии, функции коры больших полушарий головного мозга угасают. Человек погибает, если его жизнь не поддерживается с помощью аппарата искусственного дыхания и средствами для тонизирования сердечно-сосудистой деятельности.
Отдельно следует описать симптомы хронической гипоксии головного мозга к которым относятся:
- Повышенная утомляемость.
- Чрезмерная раздражительность.
- Эмоциональная несдержанность.
- Снижение интеллекта.
- Нарушения эмоционально-волевой сферы.
- Ухудшение памяти и внимания.
- Плохое настроение.
- Повышенная плаксивость.
- Апатия.
- Чаще всего люди становятся безучастными ко всему происходящему, реже они благодушны и находятся в эйфории.
- Часто человек испытывает головные боли, головокружения.
- Возможны периодические приступы тошноты.
- Ночной отдых нарушен, а днем человек испытывает приступы сонливости. Засыпает он с трудом, сон поверхностный, прерывистый. Часто больному снятся кошмарные сновидения. После ночи человек чувствует себя уставшим и не отдохнувшим.
- Для хронической гипоксии характерны вегетативные нарушения, среди которых: усиление пульсации в голове, появление шума в ушах, частые эпизоды потемнения в глазах, ощущение прилива жара к голове. Сердцебиение учащается, возможно появление болей в сердце и одышки. Не исключены даже эпизоды потери сознания.
Описание эксперимента и результаты
Для более точной визуализации транспорта веществ в мозг через носовую полость мы использовали наночастицы оксида марганца (Mn3O4, диаметр ~34 нм). Введя их в одну ноздрю мыши, можно увидеть положение наночастиц при томографии (рис. 3).
Рисунок 3. Томограмма обонятельной луковицы мыши.
(a) — распределение МРТ сигнала по слоям обонятельной луковицы (MOB): гломерулярному слою (GL), наружному плексиформному слою (EPL), слою митральных клеток (ML), слою зернистых клеток (GrL) спустя 24 часа после введения Mn3O4-наночастиц в правую ноздрю. Интенсивность сигнала выделена с помощью псевдоокрашивания (компьютер окрашивает изображение в различные цвета в зависимости от интенсивности МРТ-сигнала). (б) — снимок в присутствии (LTT) и отсутствии (vehicle) ингибитора пресинаптической активности нейрона. Белыми стрелками показаны слои: гломерулярный слой (GL) и слой митральных клеток (ML).
рисунок автора статьи
В ходе работы было проанализировано влияние различных ингибиторов на захват и транспорт наночастиц в головной мозг мыши для ответа на основной вопрос: наночастицы проходят из носовой полости по нейронам или они попадают в нервную систему через внеклеточное пространство [13].
Чтобы проследить путь наночастиц из обонятельного эпителия в обонятельную луковицу, были использованы специфические и неспецифические ингибиторы эндоцитоза, а также вещества, разрушающие плотные контакты клеток обонятельного эпителия. Отличия между ингибиторами эндоцитоза в том, что специфические ингибиторы блокируют захват клетками определенного вещества, а неспецифические снижают общую способность клеток к эндоцитозу. Исходя из полученных данных, мы заключили, что частицы поглощаются клетками ольфакторного эпителия, а не проходят между ними. Также можно сделать вывод, что захват наночастиц происходит без сопряжения с каким-либо веществом, так как специфические ингибиторы эндоцитоза не влияли на уровень МРТ-сигнала.
Чтобы проследить дальнейший путь наночастиц, мы использовали ингибиторы аксонального транспорта (колхицин, лидокаин). Колхицин блокирует перемещение грузов от тела нейронов до синапса; лидокаин подавляет проведение импульсов в нейронах вследствие блокирования натриевых каналов (поэтому наночастицы, попав в нейрон, не могут передаваться дальше в синапс). Оба ингибитора достоверно повлияли на транспорт Mn3O4-наночастиц из носовой полости в мозг. Таким образом, мы показали, что Mn3O4-наночастицы проникают в обонятельную луковицу через аксон, а их транспорт зависит от активности нейрона.
Продолжая двигаться в мозг с наночастицами, мы попадаем во внешний слой обонятельной луковицы. Здесь наночастицы стоят перед выбором: либо идти через синапс в следующий нейрон и дальше транспортироваться по латеральному обонятельному тракту, либо перемещаться через межклеточное пространство.
Понять это возможно посредством влияния блокаторов. Ингибиторы пре- и постсинаптической активности нейронов влияют лишь на стадию транспорта наночастиц из обонятельной луковицы (MOB) в латеральный обонятельный тракт (LOT). Причем значительное влияние оказывают только ингибиторы пресинаптической активности — баклофен и LTT (левитриацетам). Такой эффект появляется из-за того, что наночастицы не работают как нейромедиаторы. Чтобы вызвать у нейрона постсинаптическую активность, вещество должно связаться с рецептором на поверхности нейрона и вызвать появление потенциала действия в нем (передать сигнал дальше по нервной цепочке). Наночастицы не могут связываться со специфическими рецепторами; они попадают в следующий нейрон за счет неспецифического эндоцитоза. Из-за этого ингибиторы постсинаптической активности практически никак не влияют на транспорт наночастиц из обонятельной луковицы в латеральный обонятельный тракт. Поэтому можем сделать вывод: наночастицы передаются транссинаптически по структурам головного мозга, отвечающим за обоняние в обход ГЭБ.
Чем опасна гипоксия головного мозга?
Даже легкая гипоксия головного мозга – это опасное для здоровья состояние, которое приводит к патологическим изменениям, оказывающим влияние на весь организм в целом. Чем сильнее кислородное голодание, тем тяжелее его последствия. Прогноз зависит от того, какова степень повреждения тканей головного мозга и как долго длилась гипоксия.
Если человек впал в кому на кратковременный период времени, то шансы на полноценную реабилитацию достаточно высоки. Если больной не был в коме, то восстановится он еще быстрее (при условии оказания адекватной и своевременной медицинской помощи).
Если человек долгое время пребывал в коме, но вышел из нее, то такое состояние не может остаться без последствий. Продолжительность жизни таких пациентов чаще всего не превышает одного года. При этом у лежачих больных формируются пролежни, они в большей степени подвержены инфекционным заболеваниям, возбудителями которых становятся больничные штаммы бактерий. Они отличаются повышенной устойчивостью к проводимой терапии. У обездвиженных больных повышается риск формирования тромбов в венах.
После перенесенной клинической смерти человек может утратить ряд неврологических функций.
Прогноз может быть следующим:
- Полноценное восстановление мозговых функций и нормализация состояния может произойти за несколько дней или месяцев, если ткани головного мозга не подверглись разрушению. При этом пациент на протяжении всего реабилитационного периода будет испытывать астенический синдром. Иногда после значительного улучшения самочувствия может случиться его вторичное ухудшение, при этом неврологические нарушения будут стойкими.
- Частичное восстановление неврологических функций наблюдается при отмирании некоторых клеток головного мозга. Реабилитация и возвращение больного к привычной жизни происходит медленно. Некоторые функции могут не восстановиться вовсе.
Полное восстановление наблюдается редко, но если лечение проводится верно, то можно достичь устойчивой ремиссии.
Клетки головного мозга после перенесенной гипоксии не восстанавливаются, тем не менее, добиться нормализации состояния организма можно. Головной мозг обладает способностью перенимать функции соседних клеток, но частично. Поэтому помощь при гипоксии должна быть незамедлительной. В противном случае осложнения и последствия кислородного голодания головного мозга будут критичными.
Гипоксия плода
Необходимо упомянуть о такой проблеме, как гипоксия плода. Это опасное состояние, при котором плод недополучает кислород. Последствия кислородного голодания для малыша катастрофические: нарушается формирование тканей и органов, возникают повреждения мозга и центральной нервной системы. Опасность гипоксии зависит от ее степени, а также от того срока, на котором находится плод. В любом случае беременным женщинам стоит внимательнее следить за своим самочувствием и признаками гипоксии, чтобы не допустить опасных осложнений.
Диагностика гипоксии головного мозга
Для того, чтобы диагностировать гипоксию головного мозга, возможно использование следующих инструментально-лабораторных методов:
- Забор крови на общий и газовый анализ.
- Выполнение энцефалограммы головы.
- Проведение реовазографии, которая дает информацию о состоянии сосудов головного мозга.
- Общая или селективная ангиография, которая позволяет оценить кровоток головного мозга.
- МРТ – один из наиболее информативных методов исследования, который дает максимальное количество сведений о состоянии головного мозга.
- Капнография, которая позволяет определить количество углекислого газа в выдыхаемом человеком воздухе. Этот метод дает уточнить роль легких в плане развития гипоксии головного мозга.
Кроме того, врач оценивает состояние больного, необходимо определить у него наличие одышки и тахикардии. Немаловажное значение имеет осмотр пациента, определение рефлексов и прочих симптомов, характеризующих данное состояние. Для уточнения причин, которые могли спровоцировать гипоксию, нужно выяснить, имеются ли у больного заболевания внутренних органов, переносил ли он инсульт и пр.
Лечение гипоксии головного мозга
Так как гипоксия головного мозга чаще всего связана с рядом факторов, то необходимо проведение комплексной терапии, которая зависит от причины, приведшей к данному патологическому состоянию.
Если гипоксия стала следствием недостатка кислорода во вдыхаемом воздухе, то человека следует как можно быстрее перевести на дыхание нормальным воздухом. При условии, что клетки головного мозга не подверглись разрушению, то восстановление не займет много времени, а все функциональные нарушения будут устранены. Иногда больным показано добавление к обычному кислороду 3-7%-ого углекислого газа. Это позволит расширить сосуды головного мозга, простимулирует работу дыхательного центра.
При условии, что в дыхательных путях имеется посторонний предмет или иное препятствие, может потребоваться интубация трахеи и трахеотомия. Больному придают положение, которое способствует облегчению дыхания.
При выраженной дыхательной недостаточности, либо при полном отсутствии дыхания необходимо вспомогательное или искусственное дыхание, выполнение искусственной вентиляции легких. Оксигенотерапия должна быть непрерывной и продолжительной, пока в ней не отпадет необходимость.
Переливание крови, назначение сердечных и гипертензивных препаратов требуется при циркуляторной гипоксии. В этом случае важно нормализовать кровообращение. Если у больного произошла остановка сердца, требуется его непрямой массаж, применение дефибриллятора. Врач может ввести адреналин, атропин и предпринять иные реанимационные меры. Все эти мероприятия должны быть максимально быстрыми, поэтому не исключено их проведение еще в карете скорой помощи.
Для лечения и профилактики гипоксии головного мозга могут быть применены лекарственные препараты с антигипоксическим эффектом. Это наркотические и нейролептические средства, препараты для уменьшения температуры тела и пр. Иногда помочь могут глюкокортикоиды.
Обязательно нужно восстановить кислотно-щелочной и электролитный баланс в организме, однако это уже относится к симптоматическому лечению. Снять судороги позволяет Седуксен, который вводят внутривенно. Если это не помогает, то показано введение мышечных релаксантов.
Для устранения последствий гипоксии головного мозга возможно использование таких препаратов, как:
- Дибазол.
- Галантамин.
- Оксибутират натрия.
- Неробол.
- Пиридоксин.
- Церебролизин.
- АТФ.
- Транквилизаторы.
- Витаминно-минеральные комплексы.
Больной обязательно должен будет посещать кабинет массажиста и выполнять лечебные гимнастические комплексы.
Первая помощь человеку с гипоксией головного мозга
Единственное, что может сделать человек, который не обладает медицинским образованием для пострадавшего с гипоксией головного мозга – это обеспечить ему приток свежего воздуха и максимально быстро вызвать скорую помощь. До момента приезда врачей следует проветривать помещение, снять с пострадавшего все элементы одежды, мешающих дыханию.