Дата:
22 февраля 2021
Автор:
Aleksander Prejbisz, Sylwia Kołodziejczyk‑Kruk, Piotr Dobrowolski, Andrzej Januszewicz
Дополнительная информация
Для цитирования:
Prejbisz A., Kołodziejczyk‑Kruk S., Dobrowolski P., Januszewicz A.: Diagnostyka i leczenie hiperaldosteronizmu pierwotnego. Podsumowanie stanowiska European Society of Hypertension 2021. Med. Prakt., 2020; 11: 32–40
Сокращения: АГ — артериальная гипертензия, АМР — антагонист минералокортикоидных рецепторов, АРП — активность ренина плазмы, АРС — альдостерон-рениновое соотношение, КТ — компьютерная томография, ПГА — первичный гиперальдостеронизм, ФП — фибрилляция предсердий, DRC (direct renin concentration) — концентрация ренина, ESH — European Society of Hypertension
Частота встречаемости первичного гиперальдостеронизма и его клиническая картина
Частота встречаемости ПГА оценивается в 3,2–12,7 % среди пациентов первичной медико-санитарной помощи и 1–30 % среди пациентов специализированной помощи. Авторы позиции ESH указывают, что существует континуум между т. н. первичной низкорениновой артериальной гипертензией (АГ) и ПГА. ПГА — прогрессирующее заболевание, которое начинается с фазы с нормальным артериальным давлением, но со сниженной концентрацией ренина в плазме и незначительно повышенной концентрацией альдостерона, и постепенно прогрессирует до фазы с АГ и более выраженными изменениями гормонального фона.
2.Причины
Альдостерон – один из гормонов, вырабатываемых надпочечниками. Как и другие гормоны, альдостерон участвует в регуляции одновременно нескольких физиологических процессов: в частности, к основным его функциям относится поддержание нормального артериального давления, кислотно-щелочного и водно-солевого баланса (необходимой концентрации ионов натрия и калия). В строгом изначальном значении термина, синдром Конна обусловлен гормонпродуцирующей опухолью надпочечников, секреторная активность которой приводит к аномально высокому содержанию альдостерона. В основе работ Дж.Конна лежит причинно-следственная связь между удалением подобной доброкачественной опухоли (альдостеромы), с одной стороны, и, с другой, – последующей нормализацией ряда показателей у прооперированных пациентов.
В настоящее время к первичному гиперальдостеронизму, т.е. синдрому Конна, относят не только те симптомокомплексы, что обусловлены доброкачественными опухолевыми процессами в надпочечниках. Аналогичную клиническую картину может давать также гиперплазия (т.е. неонкологическое разрастание, увеличение надпочечников в размерах, которое выявляется примерно в половине всех случаев), рак надпочечника (обнаруживается менее чем в 1% случаев), генетически обусловленная гиперпродукция альдостерона обоими надпочечниками (также около 1% всех случаев первичного альдостеронизма).
Посетите нашу страницу Эндокринология
У кого следует заподозрить первичный гиперальдостеронизм
Резистентная АГ и АГ 3 степени: частота встречаемости ПГA увеличивается с ростом степени тяжести АГ. Считается, что до 20 % пациентов с резистентной АГ страдают ПГА.
АГ в молодом возрасте: пациенты в молодом возрасте (<40 лет) могут иметь более легкие формы ПГА, и иногда у них нет классических показаний для диагностики ПГА. Эта группа пациентов может получить значительную пользу от диагностики и лечения ПГА с точки зрения сердечно-сосудистого риска и качества жизни, хотя данных, подтверждающих эту гипотезу, недостаточно.
Гипокалиемия: в многочисленных исследованиях оценивалась распространенность гипокалиемии у пациентов с ПГА, но частота ПГА у пациентов с АГ и гипокалиемией не исследовалась. Тем не менее, обнаружение гипокалиемии у пациента с АГ (без иной известной причины) всегда должно вызывать подозрение на ПГА. Это также относится к гипокалиемии, вызванной диуретиками.
Инциденталома надпочечника: по оценкам, ПГА встречается у 1,6–4,3 % пациентов с инциденталомами надпочечников (в группе людей с АГ и без нее). У пациентов с инциденталомой надпочечника и АГ ПГА может встречаться чаще.
Первичный гиперальдостеронизм или инсульт в раннем возрасте в семейном анамнезе: семейные формы ПГА встречаются очень редко. Их подозрение может быть связано с инсультом в раннем возрасте у родственника 1-й степени или диагнозом ПГА у родственника 1-й степени в анамнезе. Семейную форму ПГА следует подозревать только в том случае, если ПГА обнаружен в семейном анамнезе у родственников в молодом возрасте. Из-за относительно частого возникновения ПГА, его появление у пожилых родственников может быть случайным и не обязательно указывать на генетическую предрасположенность.
Сахарный диабет, метаболический синдром и синдром обструктивного апноэ сна: авторы позиции ESH указывают, что нарушения метаболизма глюкозы, в том числе сахарный диабет, чаще встречаются у пациентов с ПГА, чем в общей популяции пациентов с АГ. Что касается синдрома обструктивного апноэ сна, было подчеркнуто, что подавляющее большинство пациентов с синдромом обструктивного апноэ сна, страдающих ПГА, имеют какое-либо из показаний для диагностики ПГА, перечисленных в документе.
Фибрилляция предсердий (ФП) значительно чаще встречается у пациентов с ПГА, чем в общей популяцией пациентов с АГ. Результаты исследования, в которое вошли пациенты с ФП, не связанной со структурным заболеванием сердца или другим заболеванием, указывают на относительно высокую долю пациентов с ПГА в этой группе (42 %).4 Однако к результатам этого исследования следует подходить с осторожностью, поскольку критерии включения пациентов с ФП неясной этиологии вызывают некоторые сомнения — в исследование были включены только 18 % пациентов из популяции пациентов с ФП и АГ, хотя в то же время авторы пришли к выводу, что само сосуществование АГ не объясняет возникновения ФП. Неясные критерии включения могут влиять на нерепрезентативность оцениваемой популяции и затрудненную экстраполяцию результатов на всю популяцию пациентов с ФП.
Скрининг на первичный альдостеронизм
В качестве скринингового теста у пациентов с подозрением на ПГА рекомендуется определить концентрацию альдостерона и ренина в плазме, а затем рассчитать альдостерон-рениновое соотношение (АРС; соотношение концентраций альдостерона и ренина в плазме), которое до сих пор считается наиболее надежным и доступным скрининговым методом. Существующие различия в методах определения концентрации ренина (DRC), активности ренина плазмы (АРП) и альдостерона не позволяют установить единую точку отсечения для АРС; в случае концентрации альдостерона, выраженной в нг/дл и АРП в единицах нг/мл/ч, наиболее часто используемая точка отсечения для АРС составляет 30 (но допустимы также значения в диапазоне 20–40) — см. табл. Поэтому отдельные лаборатории и учреждения разрабатывают собственные нормы.
Таблица. Точки отсечения для альдостерон-ренинового соотношения (АРС) как показания для дальнейшей диагностики в зависимости от метода измерения и принятых единиц определения ренина и концентрации альдостерона в плазме
| АРП (нг/мл/ч) | DRC (мМЕ/л) | |
| концентрация альдостерона (нг/дл) | 20 | 1,3 |
| 30 | 2 | |
| 40 | 2,7 | |
| концентрация альдостерона (пмоль/л) | 550 | 36 |
| 830 | 55 | |
| 1100 | 74 | |
| АРП – активность ренина плазмы, DRC – концентрация ренина на основе позиции ESH1 | ||
Концентрацию альдостерона и ренина в плазме лучше всего определять после отмены влияющих на них лекарственных средств. При необходимости пациент может принимать верапамил, доксазозин и моксонидин. Если лекарственные средства, влияющие на уровень альдостерона и ренина (β-блокаторы, дигидропиридиновые блокаторы кальциевых каналов, диуретики, ингибиторы ангиотензинпревращающего фермента, антагонисты рецепторов ангиотензина [сартаны]) не могут быть отменены, следует оценить АРС и интерпретировать результат, учитывая эффект лекарств, принимаемых пациентом. Этот тест не следует проводить пациентам, принимающим антагонист альдостерона. Перед определением концентрации альдостерона и ренина следует скорректировать гипокалиемию без ограничения потребления натрия. Образцы крови следует брать до полудня у пациента в положении сидя, по крайней мере, через 2 часа пребывания в вертикальном положении (в это время пациент может сидеть, но не может лечь).
В центре, представленном авторами этой статьи, в качестве точки отсечения для АРС используется значение 30 для концентраций альдостерона и ренина, выраженных в пг/мл. Если лабораторные значения выражены в других единицах, их можно перевести в пг/мл: умножив значение концентрации альдостерона в нг/дл на 10 и разделив значение концентрации ренина в мМЕ/л на 1,67. Также следует отметить, что если АРС находится в диапазоне 20–30, анализируется клиническая картина, и на этой основе некоторые пациенты могут быть отобраны для дальнейшей диагностики ПГА.
На рисунке 1 представлены примеры интерпретации результатов определения АРС. При интерпретации следует учитывать, не повышена ли концентрация альдостерона. Вопрос не в том, превышает ли он верхнюю границу нормы, т. е. референтный интервал, принятый в данной лаборатории. Предполагается, что концентрация альдостерона должна быть >150 пг/мл (15 нг/дл), хотя некоторые авторы рекомендуют считать точкой отсечения 100 пг/мл или граничное значение для диагностики ПГА в подтверждающем тесте (т. е. >100 пг/мл или >60 пг/мл в тесте с натриевой нагрузкой). Концентрация ренина должна быть низкой, то есть ниже или близкой к нижней границе референсного диапазона.
Рисунок -1. Альдостерон-рениновое соотношение (АРС) — скрининговая оценка в направлении первичного гиперальдостеронизма (ПГА). Пример интерпретации соотношения на основе позиции ESH от 2021 года и собственного опыта авторов данной статьи
Исследования, подтверждающие диагноз первичного гиперальдостеронизма
Положительный результат АРС обязывает провести одно из признанных исследований, подтверждающих ПГА, однако авторы позиции ESH предлагают, что у пациентов с идиопатической гипокалиемией, концентрацией ренина в плазме ниже порога обнаружения или очень низкой и с концентрацией альдостерона в состоянии покоя >200 пг/мл (20 нг/дл) ПГА можно диагностировать без необходимости проведения подтверждающего исследования.
В позиции ESH перечислены 4 наиболее часто используемые подтверждающие исследования: пероральный и внутривенный тест с натриевой нагрузкой, тест с каптоприлом и тест с флудрокортизоном, при этом подчеркивается, что выбор метода должен зависеть от доступности данного метода и опыта конкретного учреждения. Как и в случае определения АРС, следует учесть лекарственные средства, влияющие на ренин-ангиотензин-альдостероновую систему, и оценить противопоказания к проведению исследования — в случае теста с натриевой нагрузкой это: значительно повышенное артериальное давление, тяжелые сердечная недостаточность и почечная недостаточность.
Авторы позиции ESH обсуждали возможность рекомендации одного теста и граничных значений для диагностики ПГА. Из-за отсутствия достаточных данных не было принято решение о конкретных значениях. На рисунке 2 предложен диагностический алгоритм ПГА, разработанный на основе обсуждаемой позиции и опыта авторов данной статьи. На практике в настоящее время наиболее часто используемым тестом является тест с натриевой нагрузкой в положении сидя. Наиболее часто используемым пороговым значением, позволяющим диагностировать ПГА в этом случае, является концентрация альдостерона >60 пг/мл (170 нмоль/л) с концентрацией кортизола ниже после инфузии 0,9 % раствора NaCl, чем определенная изначально. Приняты также пороговые значения для теста с натриевой нагрузкой в положении лежа: >100 пг/мл (точный диагноз) и 50–100 пг/мл (вероятный диагноз). В позиции ESH указано, что тест с натриевой нагрузкой, выполняемый в положении сидя, может быть предпочтительным методом, а в случае противопоказаний к его проведению может быть проведен тест с каптоприлом.
Рисунок -2. Алгоритм диагностической тактики у людей с подозрением на первичный гиперальдостеронизм. Приведенные граничные значения на отдельных этапах диагностики были предложены на основании позиции ESH и опыта авторов данной статьи. Их следует рассматривать как примеры и учитывать используемую методологию и опыт данного учреждения
Дифференциация форм первичного гиперальдостеронизма
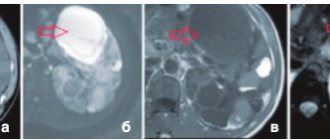
Компьютерная томография
Всем пациентам с ПГА следует проводить компьютерную томографию (КТ) брюшной полости с контрастированием для исключения рака надпочечников и оценки венозного оттока перед катетеризацией надпочечниковых вен, а у пациентов, отобранных к операции, — анатомическую оценку перед адреналэктомией.
Авторы позиции ESH подчеркивают, что соответствие результатов КТ результатам, полученным на основании катетеризации надпочечниковых вен, не является удовлетворительным. Самый крупный метаанализ, проведенный на сегодняшний день, включающий 38 исследований и в общей сложности 950 пациентов с ПГА, показал, что результат визуализирующего исследования (КТ или МРТ) почти в 38 % случаев отличался от результата катетеризации надпочечниковых вен. Следует отметить, что анатомическое изображение надпочечников не может определять диагноз ПГА и дифференциацию его формы. Наличие двусторонней гиперплазии коры надпочечников при визуализирующем исследовании не указывает на наличие ПГА. Необходимо провести гормональные анализы. Так же обнаружение аденомы у пациента с ПГА (при КТ) не определяет диагноз односторонней формы (за исключением конкретной клинической картины, описанной ниже).
Катетеризация надпочечниковых вен
Определение формы ПГА имеет ключевое значение при выборе метода лечения. У всех пациентов с односторонней формой заболевания, соответствующим образом отобранных к операции, адреналэктомия нормализует уровень калия в сыворотке крови, у 30–60 % пациентов вызывает нормотензию без необходимости приема гипотензивных лекарственных средств, а у остальных пациентов улучшает контроль артериального давления. С другой стороны, пациентам с двусторонней формой ПГА адреналэктомия не приносит такой пользы, и их следует лечить фармакологически.
В позиции ESH по-прежнему подчеркивается важность катетеризации надпочечниковых вен как «золотого стандарта» в определении формы ПГА. Авторы подробно обсуждают принципы выполнения этой процедуры и интерпретации результатов – заинтересованным мы рекомендуем обратиться к этому документу.2
Молодым пациентам (<35 лет) с идиопатической гипокалиемией, значительно увеличенной секрецией альдостерона (концентрация альдостерона в плазме >300 пг/мл), типичной картиной односторонней аденомы (> 10 мм) на КТ и нормальным морфологическим изображением второго надпочечника, может не требоваться катетеризация надпочечниковых вен перед адреналэктомией.
4.Лечение
Очевидно, что терапевтическая стратегия в каждом случае определяется диагностированными причинами гиперальдостеронизма. Так, при односторонней альдостероме методом выбора является лапароскопическая адреналэктомия; эффективность хирургического вмешательства в данном случае очень высока – практически у всех пациентов постепенно нормализуется давление и прочие связанные с альдостероном показатели.
В других случаях предпочтительным может оказаться консервативное лечение, главной задачей которого является предотвращение тяжелых осложнений, вызванных гипертензией и гипокалиемией. Назначают специальные калийсохраняющие препараты, гипотензивные средства, ингибиторы АПФ, особую диету. В некоторых случаях показана и эффективна гормональная терапия (дексаметазон, гидрокортизон). Необходимыми мерами являются также нормализация массы тела, лечебные упражнения на воздухе.
Лечение первичного гиперальдостеронизма
Пациенты с ПГА характеризуются повышенным риском осложнений со стороны сердечно-сосудистой системы по сравнению с пациентами с идиопатической АГ, что связано не только с длительными эффектами повышенного артериального давления, но и с повреждающим действием самого избытка альдостерона. И адреналэктомия, и медикаментозная терапия антагонистами минералокортикоидных рецепторов (АМР) снижают этот риск.
В позиции ESH рекомендуется выполнять одностороннюю лапароскопическую адреналэктомию людям с документально подтвержденной односторонней формой заболевания. Остальным пациентам следует проводить постоянное фармакологическое лечение с помощью АМР. Это лечение также следует добавить у пациентов с положительным результатом скринингового теста (АРС), которые не согласны продолжать диагностику или которым она противопоказано.
У пациентов с двусторонней формой ПГА лечением выбора является спиронолактон, а в случае его непереносимости — эплеренон. Дозу лекарства следует постепенно увеличивать. Считается, что оптимальная доза АМР должна обеспечить нормокалиемию без необходимости восполнения калия. Также считается, что снижение частоты сердечно-сосудистых осложнений при ПГА достигается только при наличии полной блокады минералокортикоидных рецепторов, о чем свидетельствует не сниженная концентрация ренина.5 При неуверенности в применяемой дозе, следует измерить концентрацию ренина — если она все еще низкая, это означает, что полная блокада рецепторов не произошла и дозу следует увеличить.
Использование эплеренона ограничено отсутствием регистрации для использования при АГ и ПГА в Европе. Следует помнить, что эплеренон применяется в дозе примерно в 2 раза превышающей дозу спиронолактона и в 2 приема.
Гиперальдостеронизм
Синдром, обусловленный гиперпродукцией альдостерона клубочковой зоной коры надпочечников, сопровождающийся артериальной гипертензией и миастенией.
Причиной гиперальдостеронизма
может быть гормонально активная аденома коры надпочечников (альдостерома), двусторонняя гиперплазия клубочковой зоны коры надпочечников, множественные микроаденомы коры надпочечников. Гиперальдостеронизм может развиваться при хронических заболеваниях почек, гипертонической болезни, при некоторых опухолях почек. Причиной гиперальдостеронизма может быть также длительное употребление лекарственных препаратов: мочегонных, слабительных, контрацептивов. Преходящее состояние гиперальдостеронизма наблюдается в период лютеиновой фазы менструального цикла, во время беременности, при ограничении натрия в диете.
В зависимости от причины в клинической практике различаются:
1. Альдостеронизм с низкой секрецией ренина
- Первичный альдостеронизм в результате опухоли клубочкового слоя коры надпочечников (синдром Конна).
- Идиопатический гиперальдостеронизм – диффузная гиперплазия коры надпочечников.
- Дексаметазоновый гиперальдостеронизм, подавляемый глюкокортикоидами.
- Гиперальдостеронизм, вызванный эктопическими опухолями.
2. Альдостеронизм с нормальной или повышенной секрецией ренина (вторичный гиперальдостеронизм).
- Симптоматическая артериальная гипертензия при реноваскулярной патологии, заболевании почек, гипертонической болезни.
- Ренинсекретирующие опухоли (опухоль Вильмса).
- Ятрогенный и физиологический гиперальдостеронизм.
Патогенез заболевания
связан с избыточной секрецией альдостерона. Основным действием альдостерона является регуляция реабсорбции натрия и экскреции калия в почечных канальцах. При гиперальдостеронизме развивается задержка ионов натрия и выведения калия, что сопровождается гиперкалиурией, гипокалиемией, гипернатриемией. В результате гипокалиемии возникает гипокалиемическая нефропатия, которая сопровождается полиурией, дистрофическими изменениями в мышцах, миокарде. Развитие гипертонии обусловлено задержкой натрия, накоплением его в стенках артерий, их набуханием, повышением тонуса и чувствительности к прессорным агентам. При наличии аденомы надпочечника синтез альдостерона автономен.
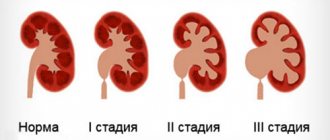
Клиническая картина.
Начальным симптомом является ранняя гипертензия. Больные жалуются на головные боли, ноющие боли в области сердца. Стадия выраженной симптоматики характеризуется нарушением зрения, мышечной слабостью, судорогами, болями в мышцах. Выражены почечные симптомы: полиурия, изогипостенурия, никтурия, вторичная полидипсия. Со стороны сердечно-сосудистой системы: нарушение сердечного ритма, тахикардия, систолическая и диастолическая артериальная гипертензия.
Диагностические критерии:
- Сочетание гипертензии и миастенического синдрома.
- Гипернатриемия, гипокалиемия, гиперкалиурия.
- Полиурия, изо- и гипостенурия. Реакция мочи щелочная.
- Увеличение уровня альдостерона в плазме и его экскреция с мочой.
- Увеличение размеров надпочечников при ультразвуковой сонографии, КТ или ангиографии.
- Признаки гипокалиемии на ЭКГ.
Для уточнения диагноза
проводятся функциональные пробы, пробы с верошпироном, с нагрузкой хлористым натрием, фуросемидом.
Лечение
зависит от причин, обусловливающих гиперальдостеронизм. При первичном гиперальдостеронизме показано хирургическое лечение. При вторичном гиперальдостеронизме осуществляется длительное медикаментозное лечение спиронолактоном, препаратами калия, ингибиторами синтеза глюкокортикоидов. Независимо от этиологии заболевания диета должна содержать ограниченное количество поваренной соли и продукты, богатые калием (картофель, курага, рис, изюм).